ESTRATIFICAÇÃO DE RISCO NAS SÍNDROMES CORONARIANAS AGUDAS,
NO PRIMEIRO ATENDIMENTO
Faculdade de Ciências Médicas — Unicamp
Endereço para correspondência:
Rua Benjamin Constant, 2050 — 7 o andar — CEP 13010-142 — Campinas — SP
INTRODUÇÃO
Os pacientes com quadro clínico compatível com síndrome coronariana aguda podem apresentar complicações cardiovasculares como óbito, infarto agudo do miocárdio, isquemia refratária ou necessidade de revascularização miocárdica de urgência. Essa população é muito heterogênea, sendo composta desde indivíduos de baixo risco até por aqueles que são de altíssimo risco de evoluírem para complicações cardiovasculares. No tratamento desses, portanto, é fundamental que o risco seja definido no momento do primeiro atendimento, para que a conduta adotada seja adequada a cada caso.
Durante o atendimento inicial ao paciente com dor torácica, duas questões fundamentais devem ser formuladas. O quadro clínico é compatível com síndrome coronariana aguda? Caso a resposta seja afirmativa, qual é o risco de que esse indivíduo venha a apresentar evento cardiovascular grave? Ao responder a essas perguntas, estarão sendo definidos o tipo de tratamento farmacológico, a necessidade de internação e uma possível estratégia invasiva.
Mais de 30% dos eventos cardiovasculares precoces (dentro dos primeiros 30 dias), após quadro isquêmico, ocorrem até o quinto dia da admissão hospitalar(1-4), envolvendo, além das complicações já mencionadas, acidente vascular encefálico, insuficiência cardíaca e arritmia grave. Durante esse período, um mesmo paciente pode evoluir para diferentes categorias de risco, o que demanda constante monitorização clínica.
Em resumo, a caracterização da gravidade de um quadro de síndrome coronariana aguda inicia-se no momento da chegada do paciente ao departamento de emergência e acompanha seu curso intra-hospitalar. É um processo extremamente dinâmico e multifatorial, do qual dependem a conduta adotada e o prognóstico de cada caso.
A NECESSIDADE DA ESTRATIFICAÇÃO DE RISCO
A estratificação de risco vem possibilitando a identificação de pacientes graves, a escolha correta do tratamento a ser dispensado e a otimização dos custos da internação hospitalar. Sua aplicação durante o atendimento inicial permite diferenciar pacientes de baixo, médio e alto risco, sendo justificada pelo fato de que a conduta a ser adotada irá diferir significativamente entre eles. Assim, indivíduos de maior gravidade deverão ter como destino uma unidade coronariana, enquanto os de menor risco poderão ser dispensados após receber tratamento numa unidade de emergência.
Já foi demonstrado(5) que a mortalidade após infarto agudo do miocárdio poderia atingir um número próximo a 30% antes da disseminação das unidades coronarianas, e que esse número foi reduzido para aproximadamente 15% com a utilização freqüente dessas unidades. Isso evidencia a importância do tratamento intensivo e a cuidadosa monitorização clínica, principalmente na prevenção de arritmias fatais. Obviamente, essa interpretação pode ser adotada ao se falar de síndromes coronarianas sem elevação do segmento ST, que é o objeto deste artigo.
Quando um paciente preenche os critérios de gravidade, deve ser alvo de tratamento agressivo. Inicialmente, essa estratégia aparenta ser onerosa, pois requer drogas de alto custo e recursos de maior complexidade tecnológica. A administração de inibidores de glicoproteína IIb/IIIa, por exemplo, pode ultrapassar a ordem de US$ 1.000,00(6). Essa nova classe de fármaco pode, de forma geral, reduzir a chance de óbito e de infarto do miocárdio em 10%(7). Uma recente análise(8) da relação custo-efetividade dessas drogas revelou que a redução de eventos é menos onerosa quando aplicada a paciente de alto risco. Por outro lado, tratar da mesma forma um indivíduo de baixo risco mostrou-se mais dispendioso e particularmente mais arriscado por causa dos efeitos adversos desses novos tratamentos.
Outro dado interessante que demonstra o impacto da estratificação de risco e da terapêutica adotada vem de uma análise recente do estudo PURSUIT(9). Uma comparação entre norte-americanos e latino-americanos que manifestaram quadros isquêmicos instáveis apontou sensível diferença na mortalidade isolada aos 30 dias. Os pacientes da América Latina morreram duas vezes mais que aqueles da América do Norte (6,8% "versus" 3,1%). Na análise multivariada, observou-se que os grupos não diferiam significativamente quanto aos fatores de risco. No entanto, os latino-americanos foram menos submetidos à cinecoronariografia e usaram menos drogas, como hipolipemiantes e inibidores de glicoproteína IIb/IIIa. Se o risco de eventos graves foi o mesmo nas duas populações estudadas, por que a diferença na terapêutica adotada? Pode-se supor que, nos países da América Latina, o subgrupo de maior risco não foi corretamente identificado ou, caso o tenha, sua gravidade não foi levada em conta no momento de optar pelo tratamento farmacológico ou intervencionista.
Fica claro que a avaliação sistemática de cada paciente que chega a um serviço de emergência tem implicações econômicas e relativas a prognóstico. Contemplar a real gravidade de cada caso é uma responsabilidade com a qual o cardiologista deve estar habituado e que se inicia durante a anamnese no pronto-socorro. A subdivisão dos pacientes em diferentes grupos de risco apóia-se, principalmente, na história, no exame físico, no eletrocardiograma e nos marcadores séricos de dano miocárdico.
AVALIAÇÃO CLÍNICA INICIAL
No momento da primeira avaliação de um doente que apresenta síndrome coronariana aguda, podemos nos deparar com algumas variáveis que sugerem quadro de alto risco cardiovascular. Tais informações são obtidas, principalmente, por meio de sintomas iniciais, perfil demográfico e exame físico do paciente.
A estratificação baseada em algoritmos e tabelas pode ser de grande utilidade e será discutida adiante. No entanto, aguardamos as novas diretrizes da Sociedade Brasileira de Cardiologia para que possamos aplicar um modelo mais adaptado à realidade e ao perfil do paciente brasileiro. De forma geral, os maiores indicativos da gravidade de síndrome coronariana aguda sem supradesnivelamento do segmento ST são:
1) Sintomas: quanto às apresentações clínicas, um quadro isquêmico agudo pode se apresentar como angina de repouso, de recente começo ou angina em crescendo. As duas últimas totalizam 20% dos casos, mas os sintomas surgidos em repouso são responsáveis por 80% das apresentações(10, 11). A dor de repouso com duração superior a 20 minutos representa quadro clínico grave, assim como a angina que ocorre após infarto agudo do miocárdio ou aquela que se desenvolve sem fatores desencadeantes extracardíacos. O tempo desde o último episódio e a ocorrência mesmo em vigência de tratamento farmacológico também são importantes na caracterização do risco elevado.
2) Dados demográficos: idade acima de 65 anos, sexo masculino, baixo peso, presença de diabete melito, hipertensão arterial sistêmica e doença arterial coronariana ou vascular periférica prévias são os antecedentes de maior peso na estratificação.
3) Exame físico: os maiores indicadores de gravidade ao exame são a presença de estertores ou edema pulmonar, taquicardia ou bradicardia, hipotensão, terceira bulha cardíaca e novo sopro ou piora de um sopro preexistente de insuficiência mitral.
Essas informações estão fundamentadas em estudos prévios e merecem alguns comentários. Ao se considerar a idade acima de 65 anos como fator de risco, vale lembrar que esse número pode variar para 70 ou 75 anos, dependendo da literatura utilizada. De qualquer forma, os pacientes mais velhos tendem a apresentar doença aterosclerótica mais extensa e grave, assim como maior prevalência de disfunção ventricular esquerda(4, 12).
Também vale ressaltar que, ao se citar o sexo masculino como antecedente para pior prognóstico, esse dado vale principalmente para angina instável. Quando a doença em questão é o infarto sem onda Q, a incidência de eventos cardiovasculares precoces é semelhante em ambos os sexos(13, 14).
Outros fatores de relevância clínica, como diabete melito, baixo peso e aumento ou diminuição da freqüência cardíaca, estão validados por grandes estudos, como o PURSUIT(15) e o ESSENCE(16, 17).
Passado esse primeiro momento do processo de estratificação, chega-se a um ponto vital: a interpretação dos exames subsidiários.
ACHADOS ELETROCARDIOGRÁFICOS
O eletrocardiograma continua sendo uma das chaves para o diagnóstico e a estimativa de prognóstico do paciente com dor torácica que chega ao departamento de emergência. O indivíduo que se apresenta com queixas sugestivas de isquemia miocárdica terá eletrocardiograma alterado em 50% das vezes. Os achados mais comuns são anormalidades da onda T, depressão do segmento ST ou elevação transitória desse segmento. Todavia, cada alteração do eletrocardiograma carrega um risco específico para eventos cardiovasculares. Os desvios transitórios do segmento ST, principalmente se maiores que 0,1 mV e com duração superior a 30 minutos, constituem o tipo de apresentação eletrocardiográfica mais grave(18, 19), podendo ocorrer em 15% a 30% dos casos. Novo desvio do segmento ST maior que 0,05 mV, inversão simétrica da onda T maior que 0,2 mV e presença de bloqueio de ramo também são achados de alto risco(4). A constatação de ondas Q maiores que 40 ms, por sugerirem infarto prévio, podem indicar doença coronariana de maior gravidade.
Existem evidências, na literatura, que apontam o eletrocardiograma como um preditor de risco independente de variáveis clínicas ou marcadores séricos(20). No entanto, o eletrocardiograma de repouso pode não refletir a natureza dinâmica do processo de trombose intracoronariana e isquemia miocárdica. Prova disso é o fato de que cerca de 5% dos doentes, com eletrocardiograma normal e que receberam alta do pronto-socorro após se queixarem de dor no peito, evoluíram com angina instável ou mesmo infarto agudo do miocárdio(21-23). A monitorização contínua do eletrocardiograma, portanto, é útil e recomendável durante as primeiras 24 horas de internação, podendo evidenciar alterações do segmento ST ou mesmo arritmias, apesar de estas serem menos comuns nas síndromes coronarianas agudas sem elevação de ST.
Tentar obter um eletrocardiograma durante o episódio de dor torácica é de vital importância. Caso o serviço não esteja capacitado para providenciar monitorização contínua, não deve ser desvalorizado o papel do eletrocardiograma seriado.
MARCADORES BIOQUÍMICOS
Outro poderoso instrumento no processo de estratificação é a utilização de marcadores bioquímicos. Atualmente, os marcadores que passam por maior número de estudos e comparações são: CKmb, troponinas, mioglobina e proteína C reativa. A dosagem de CKmb por meio do método atividade ainda é a mais difundida, provavelmente pelo seu baixo custo, já que não constitui parâmetro muito específico para a detecção de injúria miocárdica. Sabe-se, no entanto, que existem duas subformas de CKmb: a CKmb1 e a CKmb2 (esta última presente apenas no miocárdio). Quando a CKmb2 está elevada e a relação 2/1 é superior a 1,5, o método ganha em sensibilidade, mas continua pouco específico.
Já as troponinas estão, cada vez mais, ganhando aceitação como marcadores séricos de escolha. Podem ser detectadas no sangue periférico mesmo quando ainda não houve elevação dos níveis de CKmb. Acrescenta-se o fato de que existe relação quantitativa direta entre nível de troponina e evolução adversa. Alguns pacientes podem apresentar CKmb normal, mas a troponina já é detectável, denotando lesão menor ao miocárdio, o que leva esses pacientes a serem considerados como de alto risco(24). Vale lembrar que a troponina, independentemente se a T ou a I, costuma estar positiva apenas por volta de quatro a seis horas após o início dos sintomas e se mantém assim por cerca de duas semanas, o que dificulta o diagnóstico de re-infarto por meio desse marcador.
A mioglobina é muito pouco específica, mas tem elevada sensibilidade e pode ser detectada após duas horas do início dos sintomas, o que ajuda a excluir necrose miocárdica, caso esteja negativa, nas primeiras quatro a oito horas. Todavia, seu uso como preditor de eventos adversos não está bem estabelecido. A escolha de um determinado marcador como método ideal ainda recai sobre seus custos e sua disponibilidade em cada instituição. O uso combinado pode ser uma boa alternativa. Existem evidências de que o uso da subforma da CKmb em conjunto com uma troponina pode ser muito útil como método de triagem, reduzindo custos e otimizando a terapêutica adotada(25).
Quanto à proteína C reativa, esta é uma proteína de fase aguda correlacionada com a atividade inflamatória, podendo ser adicional e independente de outros marcadores, como a troponina(26). Pode ser promissora na avaliação de síndromes coronarianas agudas, mas ainda carece de grandes estudos que adotem essa conduta, baseados especificamente em seus níveis plasmáticos. Talvez o uso combinado de um marcador sérico de necrose tissular e outro de atividade inflamatória venha a ser uma boa alternativa no esforço de identificar pacientes que possam evoluir de forma desfavorável.
MODELOS DE ESTRATIFICAÇÃO DE RISCO
Frente à diversidade de apresentações e aos vários dados que podem ser usados na estimativa de risco do paciente com síndrome coronariana aguda, fica um tanto difícil chegar-se a um denominador comum. Um mesmo doente pode revelar características que impliquem mau prognóstico e possuir antecedentes que tendem a ser considerados como de baixo risco. O uso de modelos de estratificação ou escores de gravidade pode, portanto, orientar o cardiologista nessa tarefa, desde que encarados como métodos que não são infalíveis.
Desde a década de 1980, a classificação de angina instável proposta por Braunwald(27) vem sendo utilizada, estando baseada apenas em dados da história clínica. Essa classificação é de conhecimento geral há muito tempo, mas vale a pena tecer alguns comentários. Esquematicamente, é dividida em classes de gravidade dos sintomas, circunstâncias clínicas nas quais ocorre o quadro agudo, e intensidade do tratamento prévio ao episódio de dor.
1) Gravidade: pode ser de classes I, II ou III. Na classe I, existe angina de recente começo ou em crescendo, mas não há episódios de repouso; a classe II inclui dor de repouso que ocorreu há menos de um mês, mas não nas últimas 48 horas; e a classe III é definida pela dor de repouso que ocorreu dentro das últimas 48 horas.
2) Circunstâncias clínicas: neste caso, a classificação pode ser A, B ou C. Na classe A, os sintomas são desencadeados por fatores extracardíacos, como um episódio de tireotoxicose; quando não existem desencadeantes, estamos diante da classe B; já a classe C inclui aqueles pacientes que desenvolveram angina após infarto agudo do miocárdio.
3) Intensidade do tratamento: divide-se em 1, 2 ou 3. É considerada classe 1 caso os sintomas tenham ocorrido sem a presença de tratamento prévio para angina estável; a classe 2 é considerada quando há sintomas, mesmo em vigência de tratamento para angina estável; se a dor ocorre na presença de tratamento máximo, incluindo drogas como vasodilatadores endovenosos, o quadro pertence à classe 3.
Podemos, portanto, encontrar pacientes no extremo do baixo risco, que não apresentaram dor de repouso, cujo quadro clínico foi desencadeado por um fator extracardíaco como anemia e que não estava em uso de medicação antianginosa. Este seria definido como um caso de angina IA1. Por outro lado, existe aquele doente que se queixa de dor de repouso nas últimas 48 horas, sem quaisquer fatores desencadeantes e que já está internado recebendo nitroglicerina endovenosa. Este seria o extremo do alto risco, definido como angina IIIC3.
Recentemente, a classificação de Braunwald demonstrou ser útil para prever mortalidade em pacientes com angina instável submetidos a revascularização do miocárdio(28). Demonstrou-se que o risco de óbito precoce, após procedimento de revascularização, foi quatro vezes maior entre as classes IIIB e IIIC, quando comparadas a pacientes estáveis. Interessante foi o fato de que a sobrevida após seis meses foi similar entre os grupos, o que traz implícito o valor da estratificação pela classificação de Braunwald, durante o período inicial que se segue ao evento agudo.
Outra proposta interessante de estratificação é o escore TIMI de risco(29). Nessa classificação, são considerados sete fatores de risco. Para cada fator é atribuído valor 0 ou 1, caso esteja ausente ou presente no caso clínico em questão. Esses fatores são: idade superior a 65 anos, três fatores de risco concomitantes para doença arterial coronariana, lesão prévia em artéria coronária > 50%, desvio do segmento ST durante a apresentação inicial, dois ou mais eventos anginosos nas últimas 24 horas, uso de ácido acetilsalicílico nos últimos sete dias, e elevação de marcadores séricos. O risco de evento cardiovascular pode variar de 4,7% em quem somou 0 ou 1 ponto, a 40,9% em quem recebeu 6 ou 7 pontos. Essa é uma forma objetiva de analisar um quadro de síndrome coronariana sem supradesnível do ST, que merece atenção por causa de sua simplicidade.
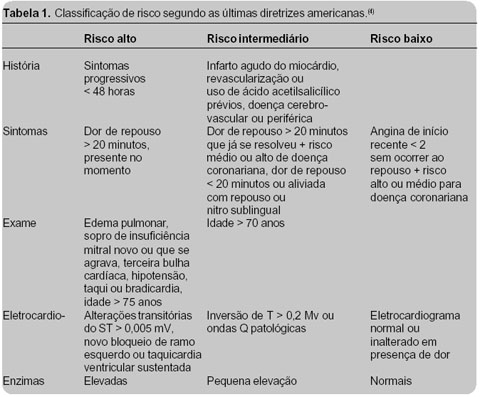
Por fim, uma forma útil e abrangente de classificação vem das últimas
diretrizes americanas(4), sendo tomada como referência em nossa
Instituição. Essa classificação divide os pacientes em três categorias de risco,
de acordo com história, sintomas, exame físico, eletrocardiograma e marcadores
bioquímicos (Tab. 1). O paciente será incluído no grupo de maior risco em que
possuir algum desses dados.
 |
REFERÊNCIAS
1. Fragmin during Instability in Coronary Artery Disease (FRISC) study group. Low-molecular-weight heparin during instability in coronary artery disease. Lancet 1996;347:561-8.
2. The RISC Group. Risk of myocardial infarction and death during treatment with low dose aspirin and intravenous heparin in men with unstable coronary artery disease. Lancet 1990;336:827-30.
3. The Global Use of Strategies to Open Occluded Coronary Arteries (GUSTO) IIb investigators. A comparison of recombinant hirudin with heparin for the treatment of acute coronary syndromes. N Engl J Med 1996;335: 775-82.
4. Braunwald E, Antman EM, Beasley JW, Califf RM, Cheitlin MD, Hochman JS, et al. ACC/AHA guidelines for the management of patients with unstable angina and non-ST-segment elevation myocardial infarction. A report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Committee on the Management of Patients with Unstable Angina). J Am Coll Cardiol 2000;36(3):970-1062.
5. Sobel BE. Coronary thrombolysis and the new biology. J Am Coll Cardiol 1989;14:850.
6. Hillegass WB, Newman AR, Raco DL. Glycoprotein IIb/IIIa receptor therapy in percutaneous coronary intervention and non-ST-segment elevation acute coronary syndromes. Estimating the economic implications. Pharmacoeconomics 2001;19(1):41-55.
7. Kong DF, Califf RM, Miller DP, et al. Clinical outcomes of therapeutic agents that block the platelet glycoprotein IIb/IIIa integrin in ischemic heart disease. Circulation 1998;98:2829.
8. Kent DM, Langa KM, Selker HP. The potential use of ECG-based prognostic instruments in clinical trials and cost-effectiveness analyses of new therapies in acute cardiac ischemia. J Electrocardiol 2000;33(suppl):263-8.
9. Cohen MG, Pacchiana CM, Corbalan R, Perez JE, Ponte CI, Oropeza ES, et al. Variation in patient management and outcomes for acute coronary syndromes in Latin America and North America: results from the Platelet IIb/IIIa in Unstable Angina: Receptor Suppression Using Integrilin Therapy (PURSUIT) trial. Am Heart J 2001;141(3):391-401.
10. Bertrand ME, Simoons ML, Fox KA, Wallentin LC, Hamm CW, McFadden E, et al. Management of acute coronary syndromes: acute coronary syndromes without persistent ST segment elevation; recommendations of the Task Force of the European Society of Cardiology. Eur Heart J 2000;21(17):1406-32.
11. van Domburg RT, van Miltenburg-van Zijl AJ, Veerhoek RJ, Simoons ML. Unstable angina: good long-term outcome after a complicated early course. J Am Coll Cardiol 1998;31 (7):1534-9.
12. Braunwald E, Mark DB, Jones RII, et al. Unstable angina: diagnosis and management. Rockville, MD: Agency for Health Care Policy and Research and the National Heart, Lung and Blood Institute, US Public Health Service, US Department of Health and Human Services; 1994:1; AHCPR Publication No. 94-0602.
13. Hochman JS, McCabe CH, Stone PH, Becker RC, Cannon CP, DeFeo-Fraulini T, et al. Outcome and profile of women and men presenting with acute coronary syndromes: a report from TIMI IIIB. TIMI Investigators. Thrombolysis in Myocardial Infarction. J Am Coll Cardiol 1997;30(1):141-8.
14. Scirica BM, Moliterno DJ, Every NR, Anderson HV, Aguirre FV, Granger CB, et al. Differences between men and women in the management of unstable angina pectoris (The GUARANTEE Registry). The GUARANTEE Investigators. Am J Cardiol 1999;84(10): 1145-50.
15. The PURSUIT Trial Investigators. Inhibition of platelet glycoprotein IIb/IIIa with eptifibatide in patients with acute coronary syndromes. The PURSUIT Trial Investigators. Platelet Glycoprotein IIb/IIIa in Unstable Angina: Receptor Suppression Using Integrilin Therapy. N Engl J Med 1998;339(7):436-43.
16. Demers C. ESSENCE trial results: breaking new ground. Efficacy and Safety of Subcutaneous Enoxaparin in Non-Q Wave Coronary Events. Can J Cardiol 1998;14(Suppl E):15E-19E.
17. Cohen M, Stinnett SS, Weatherley BD, Gurfinkel EP, Fromell GJ, Goodman SG, et al. Predictors of recurrent ischemic events and death in unstable coronary artery disease after treatment with combination antithrombotic therapy. Am Heart J 2000;139(6):962-70.
18. Langer A, Krucoff MW, Klootwijk P, Simoons ML, Granger CB, Barr A, et al. Prognostic significance of ST segment shift early after resolution of ST elevation in patients with myocardial infarction treated with thrombolytic therapy: the GUSTO-I ST Segment Monitoring Substudy. J Am Coll Cardiol 1998;31(4): 783-9.
19. Holmvang L, Andersen K, Dellborg M, Clemmensen P, Wagner G, Grande P, et al. Relative contributions of a single-admission 12-lead electrocardiogram and early 24-hour continuous electrocardiographic monitoring for early risk stratification in patients with unstable coronary artery disease. Am J Cardiol 1999;83(5):667-74.
20. Jernberg T, Lindahl B, Wallentin L. ST-segment monitoring with continuous 12-lead ECG improves early risk stratification in patients with chest pain and ECG nondiagnostic of acute myocardial infarction. J Am Coll Cardiol 1999;34(5):1413-9.
21. McCarthy BD, Wong JB, Selker HP. Detecting acute cardiac ischemia in the emergency department: a review of the literature. J Gen Intern Med 1990;5(4):365-73.
22. Rouan GW, Lee TH, Cook EF, Brand DA, Weisberg MC, Goldman L. Clinical characteristics and outcome of acute myocardial infarction in patients with initially normal or nonspecific electrocardiograms (a report from the Multicenter Chest Pain Study). Am J Cardiol 1989;64(18):1087-92.
23. Pozen M, D'Agostinho R, Selker H. A predictive instrument to improve CCU admission practices in acute ischemic heart disease. A prospective multicenter clinical trial. N Engl J Med 1984;310:1279-92.
24. Heeschen C, Hamm CW, Goldmann B, Deu A, Langenbrink L, White HD. Troponin concentrations for stratification of patients with acute coronary syndromes in relation to therapeutic efficacy of tirofiban. PRISM Study Investigators. Platelet Receptor Inhibition in Ischemic Syndrome Management. Lancet 1999;354(9192):1757-62.
25. Zimmerman J, Fromm R, Meyer D, Boudreaux A, Wun CC, Smalling R, et al. Diagnostic marker cooperative study for the diagnosis of myocardial infarction. Circulation 1999;99(13):1671-7.
26. Morrow DA, Rifai N, Antman EM, Weiner DL, McCabe CH, Cannon CP, et al. C-reactive protein is a potent predictor of mortality independently of and in combination with troponin T in acute coronary syndromes: a TIMI IIA substudy. Thrombolysis in Myocardial Infarction. J Am Coll Cardiol 1998;31(7):1460-5.
27. Braunwald E. Unstable angina: a classification. Circulation 1989;80:410-4.
28. Bjessmo S, Ivert T, Flink H, Hammar N. Early and late mortality after surgery for unstable angina in relation to Braunwald class. Am Heart J 2001;141(1):9-14.
29. Antman EM, Cohen M, Bernink PJ, McCabe CH, Horacek T, Papuchis G, et al.
The TIMI risk score for unstable angina/non-ST elevation MI: a method for
prognostication and therapeutic decision making. JAMA 2000;284 (7):835-42.