ARRITMIAS CARDÍACAS: AGENTES FARMACOLÓGICOS
Instituto do Coração (InCor) — HC-FMUSP
Endereço para correspondência:
Av. Dr. Enéas Carvalho de Aguiar, 44 — CEP 05403-000 — São Paulo — SP
INTRODUÇÃO
As arritmias cardíacas ocorrem por distúrbios na formação e/ou condução do
estímulo cardíaco. O tratamento específico das arritmias cardíacas encontra-se
indicado quando houver sintomas ou se houver benefício comprovado na redução de
morte súbita. No que diz respeito ao tratamento de emergência das arritmias
cardíacas, existe muita controvérsia quanto à escolha dos fármacos
antiarrítmicos. Desde a última diretriz proposta pelo “Advanced Cardiovascular
Life Support/American Heart Association” (ACLS/AHA), de 1992(1), uma
série de modificações foi implementada, com o peso das evidências dos grandes
estudos, a partir das Diretrizes Internacionais do ACLS 2000(2). Esta
foi a única conferência de consenso de abrangência internacional com a
finalidade específica de normatizar as condutas de ressuscitação. Dentre as
principais modificações na área de arritmias, destacam-se: a necessidade do
diagnóstico das arritmias cardíacas; a diferenciação entre a presença ou não de
cardiopatia estrutural; o uso menos freqüente de lidocaína e adenosina; a
introdução de maior arsenal de drogas antiarrítmicas, incluindo a amiodarona
endovenosa; a tentativa de diminuir os efeitos pró-arrítmicos, especialmente nos
casos de taquicardias polimórficas; e abordagem mais racional e menos
“simplista” das arritmias cardíacas. No entanto, no sentido estrito, apenas
poucas drogas antiarrítmicas estão apoiadas por fortes evidências. Obviamente,
essas mudanças implicam maior preparo técnico das equipes de emergência médica
para o reconhecimento das arritmias cardíacas específicas e de suas situações
particulares, se possível com consultoria ritmológica contínua. Assim sendo, o
modelo proposto esboça uma tentativa de conciliar o “racional” do tratamento das
arritmias cardíacas e o que as evidências da literatura têm demonstrado.
RECONHECIMENTO DAS ARRITMIAS CARDÍACAS
Algumas considerações gerais devem ser aqui mencionadas. Em
primeiro lugar, deve-se registrar um eletrocardiograma completo de 12
derivações, o que auxilia o diagnóstico, bem como a etiologia e até a
localização provável do foco arritmogênico, otimizando futura intervenção
eletrofisiológica. Deve-se sempre interpretar o eletrocardiograma e as
informações sobre o ritmo cardíaco dentro do contexto do paciente como um todo.
O diagnóstico e o tratamento inadequados costumam ocorrer quando os
profissionais da emergência tomam suas decisões baseados somente no ritmo
cardíaco e negligenciam a avaliação dos sinais clínicos do paciente, como
ventilação, oxigenação, freqüência cardíaca, pressão arterial, nível de
consciência e outros sinais de perfusão inadequada dos órgãos. As novas
Diretrizes do ACLS-2000 incluem a necessidade de os profissionais médicos
participarem de sessões contínuas de treinamento e atualização para avaliar suas
habilidades em detectar e tratar arritmias graves. É também importante que o
profissional esteja familiarizado com os equipamentos de monitorização e
diagnóstico eletrocardiográfico (como, por exemplo, desfibrilador externo,
derivação esofágica, etc.).
Os seguintes
ritmos cardíacos devem ser prontamente reconhecidos:
—
bradicardia sinusal;
— bloqueios
atrioventriculares de todos os graus;
—
extra-sístoles atriais;
—
taquicardias supraventiculares;
— arritmias
relacionadas à presença de uma via anômala (pré-excitadas);
—
extra-sístoles ventriculares;
—
taquicardias ventriculares;
— fibrilação
ventricular;
— assistolia
ventricular.
Com relação
às taquicardias, estas podem ser classificadas da seguinte forma:
a)
Taquicardias com complexo QRS estreito (supraventriculares):
—
taquicardia sinusal;
— fibrilação
atrial;
— “flutter”
atrial;
—
taquicardia atrial (ectópica e reentrante);
—
taquicardia atrial multifocal;
—
taquicardia por reentrada nodal atrioventricular;
—
taquicardia juncional;
—
taquicardia atrioventricular ortodrômica (via anômala).
b)
Taquicardias com complexo QRS largo (> 120 ms):
—
taquicardia ventricular (monomórfica ou polimórfica);
— fibrilação
ventricular;
— qualquer
taquicardia supraventricular com aberrância (bloqueio de ramo prévio ou
funcional).
c)
Taquicardias por vias anômalas (Wolff-Parkinson-White, Mahaim):
—
taquicardia atrial com condução pela via anômala;
— “flutter”
atrial ou fibrilação atrial com condução pela via anômala;
—
taquicardia atrioventricular antidrômica ou ortodrômica conduzida com aberrância.
Do ponto de
vista prático, a maioria das taquicardias com complexo QRS largo é de origem
ventricular. Além disso, se essas taquicardias ocorrerem em paciente
hemodinamicamente instável, presume-se que, até prova em contrário, devam ser
tratadas como ventriculares. É importante frisar que, em caso de parada
cardiorrespiratória, todos os cuidados preconizados pelo ACLS devem ser
priorizados em detrimento do uso das outras intervenções farmacológicas. Nos
pacientes estáveis, recomenda-se, atualmente, a necessidade de se ter
diagnóstico diferencial mais preciso das taquicardias com QRS largo. Se houver
muita dúvida, pode-se recorrer ao uso da tradicional derivação esofágica(3),
que confirmará o diagnóstico de taquicardia ventricular quando se demonstrar a
dissociação atrioventricular. Foi demonstrado que, quando os profissionais de
atendimento de emergência precisam distinguir entre taquicardia ventricular e
taquicardia supraventricular com aberrância, a possibilidade de erro ocorre em
mais de 50% dos casos. O mais freqüente é o chamado erro do tipo II, ou seja, os
médicos tendem a tratar uma real taquicardia ventricular com drogas que eles
optaram como para tratamento de taquicardia supraventricular com aberrância.(4,
5) No entanto, alguns algoritmos utilizando critérios de configuração e/ou
morfológicos do complexo QRS foram publicados(6-10), com a finalidade
de reduzir a possibilidade de erro. De acordo com as Recomendações
Internacionais do ACLS 2000, esses algoritmos são “difíceis de ensinar,
aprender, relembrar, e de ser aplicados repetidamente, e ainda podem complicar o
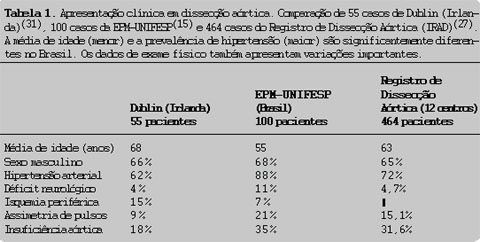
diagnóstico do infarto agudo do miocárdio”(11-13). Na visão
particular do autor, esses critérios, especialmente os critérios de Brugada(6)
(Fig. 1), quando correlacionados com os critérios morfológicos e a clínica do
paciente, são extremamente úteis. Além disso, as causas de erro do tipo II foram
publicadas numa época em que esses critérios não eram utilizados na comunidade
médica norte-americana. Outro fator que poderia influenciar os resultados seria
o volume de atendimento hospitalar de pacientes com arritmias cardíacas, e a
familiaridade dos médicos com essa doença, o que poderia aumentar a acurácia
diagnóstica em virtude do treinamento contínuo.
|
|
|
Figura 1. Algoritmo de Brugada para diagnóstico
diferencial de taquicardia com QRS largo (critérios propostos por Brugada e
colaboradores.(6)). Caso as três primeiras perguntas não possam ser
respondidas, seguir para o critério morfológico simplificado acima. |
TRATAMENTO DAS TAQUICARDIAS ESTÁVEIS COM QRS LARGO
As antigas recomendações listavam a lidocaína como droga de
escolha e, em caso de insucesso, a adenosina. As razões lógicas seriam: 1) se o
ritmo for verdadeiramente uma taquicardia ventricular, então somente a lidocaína
irá converter ao ritmo sinusal; e 2) se o ritmo for uma taquicardia
supraventricular com aberrância, então somente adenosina poderá reverter ao
ritmo sinusal. Esse conceito foi revisto por ritmologistas, que observaram o uso
exagerado da adenosina nas taquicardias com QRS largo, especialmente nos casos
de taquicardia ventricular não-responsiva à lidocaína. Esse uso inadequado da
adenosina freqüentemente causa atrasos no tratamento mais apropriado. É
importante o conceito de que a maioria das taquicardias ventriculares ocorre por
substratos anatômicos (reentrada), como na doença de Chagas, e ao redor das
cicatrizes resultantes de isquemia miocárdica. Outras drogas antiarrítmicas,
como a procainamida e a amiodarona, possuem, portanto, perfil mais adequado ao
tratamento dessas taquicardias ventriculares. Outra informação importante é que,
nas taquicardias ventriculares idiopáticas, é possível a reversão com o uso de
adenosina(14, 15), o que pode levar ao erro diagnóstico de
taquicardia supraventricular. Logo, o foco principal do tratamento das
taquicardias estáveis com QRS largo é o de primeiro se tentar o diagnóstico.
Aspectos da história clínica do paciente podem ser úteis no diagnóstico
diferencial, como: história de cardiopatia isquêmica ou outra cardiopatia
estrutural (mais provável de ser taquicardia ventricular), bloqueio de ramo
prévio ou portador de via anômala (mais provável de ser taquicardia
supraventricular).
No tratamento atual das taquicardias com QRS largo, deve-se
seguir uma seqüência de perguntas, conforme o algoritmo proposto pelas
Diretrizes do ACLS 2000. Por causa da maior complexidade do algoritmo, serão
descritos os agentes farmacológicos específicos, independentemente de serem ou
não drogas antiarrítmicas tradicionais da classificação de Vaughn Williams,
como, por exemplo, a adenosina, o sulfato de magnésio e o isoproterenol.
Lidocaína
As evidências atuais não têm apoiado o uso da lidocaína como
droga de primeira escolha para o diagnóstico e tratamento das taquicardias com
QRS largo. Alguns estudos têm demonstrado que a lidocaína é ineficaz na
supressão das taquicardias ventriculares estáveis(16, 17). Outros
estudos têm demonstrado que a lidocaína é menos eficaz que a procainamida(18)
e o sotalol endovenosos(19) na reversão das taquicardias
ventriculares. Embora a lidocaína suprima as arritmias ventriculares associadas
à isquemia miocárdica aguda ou infarto do miocárdio, o uso profilático dessa
droga foi abandonado pelo aumento da mortalidade(20).
No algoritmo atual, a lidocaína é sempre considerada droga de
segunda escolha, em 4 situações de taquicardia ventricular estável (classe IIb):
1) taquicardia ventricular monomórfica estável sem cardiopatia estrutural; 2)
taquicardia ventricular monomórfica estável com cardiopatia estrutural; 3)
taquicardia ventricular polimórfica com intervalo QT normal; e 4) taquicardia
ventricular polimórfica com intervalo QT longo. Outras situações em que o uso da
lidocaína poderia ser aceitável seriam: 1) em infartos do miocárdio
não-complicados ou isquemia, onde não se pode contar com desfibrilador ou quando
houver comprometimento hemodinâmico pela alta freqüência de extra-sístoles
ventriculares (classe indeterminada); e 2) na taquicardia ventricular ou na
fibrilação ventricular sem pulso, que persiste após a desfibrilação e a
administração de adrenalina (classe indeterminada).
Adenosina
A adenosina exerce seu principal efeito sobre a condução
nodal atrioventricular ou sobre arritmias que sejam AMPcíclico-dependentes.
Portanto, não é um agente eficaz na supressão da maioria das arritmias
ventriculares, bem como nas arritmias atriais associadas à pré-excitação
ventricular.(21, 22). Somente deve ser utilizada quando a taquicardia
de complexo QRS largo for comprovadamente de origem supraventricular. Seu uso no
diagnóstico diferencial das taquicardias de complexo QRS largo deve ser
desencorajado, pois pode ser deletério no caso de pré-excitação com condução
anterógrada(23) ou retardar o tratamento adequado de uma taquicardia
ventricular. A adenosina também pode causar angina e broncoespasmo(23).
Felizmente, a adenosina possui meia-vida inferior a 5 segundos. A dose inicial
recomendada é de 6 mg por via endovenosa em bolo rápido por 1 a 3 segundos,
podendo ser seguida por "flush" de 20 ml de solução salina. Em caso de insucesso
em 1 a 2 minutos, administram-se 12 mg do mesmo modo.
A adenosina possui várias interações medicamentosas. A
teofilina ou derivados das xantinas bloqueiam o receptor responsável pelos
efeitos eletrofisiológicos e hemodinâmicos da adenosina. Os efeitos da adenosina
são potencializados pelo dipiridamol, pela carbamazepina e em pacientes
denervados pelo transplante cardíaco.
Procainamida
A procainamida, droga antiarrítmica do grupo I-A, é eficaz no
tratamento tanto de arritmias ventriculares como supraventriculares (com ou sem
aberrância)(18, 24). É também ótima opção para o tratamento das
arritmias relacionadas à presença de uma via anômala (classe IIa), pois bloqueia
tanto o componente retrógrado como o anterógrado da taquicardia.(25, 26)
Amiodarona
Nenhuma droga antiarrítmica mereceu tanta atenção nos últimos
anos como a amiodarona, tanto sobre seus efeitos eletrofisiológicos, como pelos
seus efeitos não relacionados à ação antiarrítmica "per se". Além da eficácia na
maioria das arritmias cardíacas, mesmo nos casos de disfunção ventricular,
várias publicações científicas têm demonstrado sua eficácia na prevenção de
eventos cardíacos fatais em pacientes de alto risco(27-31).
Conseqüentemente, a introdução da amiodarona como droga em emergências
cardiológicas foi uma das grandes modificações nas novas diretrizes
internacionais do ACLS 2000. A amiodarona também é segura e eficaz nas
taquicardias supraventriculares com QRS largo, porque bloqueia a condução pela
via acessória (classe IIa se a função ventricular esquerda for normal; classe
IIb se a função ventricular esquerda for comprometida). A amiodarona é o
antiarrítmico de escolha (após insucesso da adenosina) em pacientes com
taquicardia supraventricular estável, com aberrância, se a fração de ejeção do
ventrículo esquerdo for menor que 40% ou se houver sinais de insuficiência
cardíaca.
A amiodarona não tem sido estudada especificamente para a
supressão farmacológica de taquicardia ventricular estável, porém seu uso
endovenoso tem se mostrado eficaz no tratamento das taquicardias ventriculares
instáveis e da fibrilação ventricular(32-37). Apesar do potencial
efeito inotrópico negativo, a amiodarona, hemodinamicamente, é mais bem tolerada
que a procainamida(38). A amiodarona é uma ótima opção de escolha nas
taquicardias ventriculares estáveis em portadores de insuficiência cardíaca
congestiva. Se não houver resposta com a amiodarona, a próxima intervenção a ser
tentada é a cardioversão elétrica. Dentro dos princípios de ser o menos
prejudicial ao paciente, deve-se evitar usar mais que um agente antiarrítmico,
especialmente nos portadores de cardiopatia estrutural, nos quais o risco de
pró-arritmia é bem maior.
Outras drogas antiarrítmicas
O sotalol, a flecainida e a propafenona, administrados por
via endovenosa, são drogas que, embora eficazes na supressão de arritmias
ventriculares e supraventriculares (com ou sem pré-excitação), não têm sido
estudadas no tratamento das taquicardias com QRS largo. Também são drogas de
difícil disponibilidade (no Brasil não existem, comercialmente, nem o sotalol
nem a flecainida para administração por via intravenosa). Além disso, as drogas
do grupo Ic devem ser evitadas em pacientes com cardiopatia isquêmica, devido ao
aumento da mortalidade.
RESUMO DO TRATAMENTO DAS TAQUICARDIAS DE COMPLEXO QRS
LARGO, HEMODINAMICAMENTE ESTÁVEIS
Após o diagnóstico diferencial das taquicardias de QRS largo
e em se confirmando o diagnóstico de taquicardia supraventricular com aberrância,
deve-se tratar de acordo com o algoritmo específico para as taquicardias com QRS
estreito (manobras vagais e adenosina por via endovenosa). De acordo com cada
ritmo específico, tratar de modo individualizado (por exemplo, "flutter" atrial
® cardioversão elétrica). Nas taquicardias com QRS largo, estão contra-indicados
a adenosina, os bloqueadores de cálcio e os betabloqueadores, pois, em caso de
arritmia por pré-excitação ventricular (condução anterógrada), essas drogas
teriam o potencial de ser deletérias.
Se o diagnóstico for de taquicardia ventricular ou se o
diagnóstico for genérico (taquicardia de QRS largo de origem não-esclarecida), a
cardioversão elétrica (classe I) é o tratamento mais seguro, embora possa não
ser possível, desejável ou bem-sucedido. Assim, as drogas antiarrítmicas
recomendadas seriam a amiodarona (classe IIb) ou a procainamida (classe IIa). De
acordo com as diretrizes internacionais do ACLS 2000, em caso de taquicardia
ventricular monomórfica estável, qualquer uma dessas drogas deve ser preferível
à lidocaína: amiodarona por via endovenosa (classe IIb), procainamida por via
endovenosa (classe IIa), sotalol por via endovenosa (classe IIa) ou
betabloqueadores por via endovenosa. Embora a lidocaína possa ser administrada
rapidamente, com mínimos efeitos sobre a pressão arterial, os estudos têm
sugerido que essa droga é relativamente ineficaz para a supressão das
taquicardias ventriculares(16, 17), e menos efetiva na reversão das
taquicardias ventriculares que a procainamida(18) e o sotalol(19).
Em caso de taquicardia ventricular monomórfica com disfunção ventricular, a
amiodarona por via endovenosa é a droga de escolha (classe IIa). Em nosso meio,
devido à grande incidência de doença de Chagas, temos observado excelentes
resultados na supressão das taquicardias ventriculares com a amiodarona ou a
procainamida. No entanto, faltam trabalhos mais consistentes na literatura para
respaldar esses resultados.
TAQUICARDIA VENTRICULAR POLIMÓRFICA
As taquicardias ventriculares polimórficas, geralmente,
possuem freqüência cardíaca irregular, são hemodinamicamente instáveis e têm
alto potencial para degenerarem para fibrilação ventricular. Podem estar
associadas ou não à síndrome do QT longo congênito ou adquirido (geralmente por
drogas), situação definida como "torsades de pointes". Outra causa comum é a
ligada à isquemia aguda e aos distúrbios eletrolíticos. As taquicardias
polimórficas, incluindo o "torsades de pointes", costumam recorrer e raramente
mantêm-se estáveis.
As taquicardias ventriculares polimórficas hemodinamicamente
instáveis devem ser tratadas conforme o algoritmo de taquicardia ventricular ou
fibrilação ventricular sem pulso ("ABC" ® desfibrilação ® adrenalina). Se a
taquicardia for hemodinamicamente estável, então deve-se tratar conforme a
presença ou não de "torsades de pointes", incluindo a interrupção imediata das
medicações que prolongam o intervalo QT, e a correção de distúrbios
hidro-eletrolíticos e quaisquer outros fatores precipitantes (como, por exemplo,
bradicardia extrema). Várias drogas podem causar QT longo, e muitas delas são
mencionadas a cada publicação científica. Para se manter atualizado sobre quais
as drogas (conhecidas e recentemente descobertas) que podem causar aumento do
intervalo QT e/ou "torsades de pointes", pode-se recorrer a diversos sites na
Internet, entre eles o de uma organização internacional (SADS Foundation;
www.sads.org), e outro supervisionado pelo Prof. Peter Schwartz, uma das
maiores autoridades no assunto (www.qtsyndrome.ch/).
Outras intervenções podem ser úteis, porém ainda não foram
adequadamente testadas em estudos clínicos controlados, o que se justifica pelas
dificuldades técnicas inerentes à própria doença (rapidez no atendimento, número
pequeno de casos, aspectos éticos etc.). Dentre as opções, destacam-se o sulfato
de magnésio endovenoso (classe indeterminada) e o implante de marcapasso
provisório com "overdrive supression" (classe indeterminada)(39). Se
for descartada coronariopatia aguda ou crônica, pode-se utilizar o isoproterenol
(classe indeterminada) como medida provisória para acelerar a freqüência
cardíaca enquanto o marcapasso provisório está sendo implantado (classe
indeterminada)(40). Após o implante do marcapasso, podem-se utilizar
betabloqueadores, de preferência com ação no sistema nervoso central (como, por
exemplo, propranolol ou nadolol), pois acredita-se que mecanismos simpáticos
neuro-humorais participem de algumas formas da síndrome do QT longo. A lidocaína
tem, também, indicação classe indeterminada.
Se a taquicardia ventricular polimórfica não estiver ligada
ao "torsades de pointes", o sulfato de magnésio é ineficaz. Se for conseqüente a
síndrome coronariana aguda, recomenda-se o uso de betabloqueadores e agentes
antiisquêmicos. A lidocaína pode ser mais efetiva nesses casos de isquemia
miocárdica.(41) Outros agentes farmacológicos, nessa situação, são
considerados classe IIb ou indeterminada, porque as evidências provêm de
extrapolações a partir de resultados favoráveis no tratamento de taquicardias
ventriculares monomórficas, estáveis ou instáveis hemodinamicamente. São eles:
1) amiodarona por via endovenosa (IIb); 2) lidocaína por via endovenosa (IIb);
3) procainamida por via endovenosa (IIb); 4) sotalol por via endovenosa (IIb);
5) betabloqueadores por via endovenosa (indeterminada); ou 6) difenil-hidantoína
por via endovenosa (indeterminada).
FIBRILAÇÃO VENTRICULAR OU TAQUICARDIA VENTRICULAR SEM
PULSO
Nessa situação grave e particular, as medidas de
desfibrilação serão privilegiadas sobre a escolha de agentes antiarrítmicos. Os
choques não devem ser retardados até que haja acesso venoso e que as medicações
possam ser administradas. O número ideal de choques que devem ser aplicados
antes da terapia farmacológica ainda é desconhecido. No entanto, dada a eficácia
da desfibrilação precoce (classe I), recomenda-se iniciar a terapia
farmacológica somente após a aplicação de pelo menos três choques seqüenciais.
Os pacientes cujos ritmo e perfusão podem ser provisoriamente restaurados, mas
não totalmente mantidos entre os choques repetidos (taquicardia ventricular/fibrilação
ventricular recorrentes), são candidatos altamente apropriados para o tratamento
precoce com drogas antiarrítmicas. Os médicos cardiologistas freqüentemente
deparam-se com situações clínicas nas quais o paciente se apresenta com
arritmias ventriculares instáveis e resistentes à cardioversão elétrica ou
recorrentes após choques sucessivos.(42) A pronta implementação de
drogas antiarrítmicas, nesses pacientes, é um momento crítico, uma vez que
pequenos atrasos multiplicam as chances de resultado desfavorável. Ao mesmo
tempo, esses pacientes também requerem tratamento imediato da cardiopatia de
base, como a isquemia e a insuficiência cardíaca. Sem a preocupação com esses
problemas, o tratamento antiarrítmico irá provavelmente falhar. Uma vez
recuperados de parada cardiorrespiratória, esses pacientes tornam-se excelentes
candidatos para o uso de drogas antiarrítmicas a longo prazo, tratamento
ablativo e/ou o implante de desfibriladores.
O valor das drogas antiarrítmicas administradas
profilaticamente, após fibrilação ventricular ou taquicardia ventricular
cardiovertidas eletricamente, continua desconhecido. Em recente publicação, o
estudo ARREST(43) ("Amiodarone in the Resuscitation of REfractory
Sustained ventricular Tachyarrhythmias"), completamente randomizado,
prospectivo, duplo-cego, com controle de placebo, avaliou o uso de amiodarona
endovenosa em pacientes atendidos por parada cardiorrespiratória fora do
ambiente hospitalar, decorrente de fibrilação ventricular ou taquicardia
ventricular sem pulso. No total, 504 pacientes com parada cardiorrespiratória,
cujo primeiros três choques sucessivos foram ineficazes, foram randomizados para
receber placebo (n = 258) ou 300 mg, por via intravenosa, de amiodarona (n =
246), seguido por todas as medidas-padrão de ressuscitação cardiopulmonar, de
acordo com as diretrizes da American Heart Association. Ambos os grupos tinham
características clínicas similares, incluindo o tempo até a chegada ao hospital
(20 minutos). Os pacientes sob uso de amiodarona apresentaram mais hipotensão e
bradicardia que o grupo placebo, quando havia retorno aos parâmetros
circulatórios. Apesar disso, o grupo com amiodarona teve sobrevida admissional
hospitalar maior, com significância estatística, quando comparado com o grupo
placebo (44% "versus" 34%, respectivamente; p = 0,03). O benefício foi
consistente em todos os grupos de apresentação de parada cardiorrespiratória (fibrilação
ventricular, assistolia ou atividade elétrica sem pulso, que retornava à
fibrilação ventricular durante o tratamento). Quando ajustado para outras
variáveis e co-variáveis que pudessem afetar os resultados, o tratamento com
amiodarona confirmou ser um preditor de risco independente de sobrevida
admissional hospitalar ("odds ratio" 1,6; IC 95%, 1,1-2,4; p = 0,02). Pelas
características do delineamento desse estudo, não houve poder estatístico para
detectar diferenças de sobrevida na alta hospitalar entre os dois grupos,
embora, com tendência estatística, inconclusivamente, isso favoreça o grupo com
amiodarona. Esse estudo corroborou a evidência do uso da amiodarona por via
endovenosa, após a adrenalina, para tratar as paradas cardíacas refratárias
(classe IIb), com maior probabilidade de sucesso na ressuscitação cardíaca. A
dose recomendada é de 300 mg por via endovenosa em infusão rápida, diluídos em
20 ml a 30 ml de solução salina ou glicosada. Nos casos recorrentes, podem-se
utilizar doses suplementares de 150 mg por via endovenosa em infusão rápida e
dose de manutenção de 1 mg/min por seis horas, seguido de 0,5 mg/min, até a dose
máxima de 2 g nas 24 horas. Um fato interessante demonstrado no estudo ARREST
foi que o tempo médio desde a chegada da equipe médica até a administração da
amiodarona foi de cerca de 13 minutos. Uma vez que a administração da droga
requereu enorme tempo extra, seria inaceitável normatizar que a amiodarona fosse
utilizada idealmente antes do quarto choque. Além disso, foram aplicados, em
média, 5 choques até que a amiodarona fosse administrada, bem como 4 ou mais
choques adicionais foram aplicados após a introdução da droga.
Com relação ao uso da lidocaína, as evidências atuais não
corroboram seu uso rotineiro. Não se provou sua eficácia nem a curto nem a longo
prazos na parada cardíaca. Um estudo randomizado, comparando a lidocaína e
amiodarona, demonstrou alta probabilidade de sucesso da amiodarona na
ressuscitação cardíaca(44). Outro estudo randomizado comparou a
adrenalina com a lidocaína, e revelou alta incidência de assistolia com o uso da
lidocaína e nenhuma diferença no retorno à circulação espontânea(45).
A procainamida, em decorrência da escassez de estudos e de
sua limitação pela necessidade de infusão lenta, não tem sido recomendada na
parada cardíaca. O sulfato de magnésio pode ser benéfico, especialmente nas
taquicardias ventriculares polimórficas por "torsades de pointes". No entanto,
seu uso rotineiro na ressuscitação cardíaca não alterou os resultados a curto e
a longo prazos.
Em resumo, recomenda-se o uso de adrenalina e amiodarona por
via endovenosa (classe IIb) para tratar as paradas cardíacas refratárias ao
choque elétrico decorrentes de fibrilação ventricular ou taquicardia ventricular
sem pulso. Já a lidocaína e o magnésio (para suspeita de "torsades de pointes"
ou hipomagnesemia) podem ser considerados tratamentos alternativos (classe
indeterminada).
TAQUICARDIAS PAROXÍSTICAS SUPRAVENTRICULARES
Neste tópico, consideraremos como taquicardias paroxísticas
supraventriculares "stricto sensu" as taquicardias com intervalo RR regular, com
QRS estreito ou alargado por aberrância de condução, sem onda P sinusal
conduzida. Assim, serão incluídas as taquicardias por reentrada nodal ou as
taquicardias atrioventriculares mediadas por vias anômalas manifestas ou
ocultas. As demais taquicardias, como fibrilação, "flutter" e taquicardias
atriais, e as taquicardias juncionais serão comentadas posteriormente.
Embora a conduta inicial nas emergências não tenha sofrido
grandes alterações, muita ênfase tem sido dada à necessidade do diagnóstico
diferencial, sempre que possível. Nas taquicardias por reentrada nodal, por
causa do sentido craniocaudal da ativação e do curto intervalo RP', as ondas P
costumam estar ausentes ou se apresentar na forma de pseudo s' nas derivações
inferiores (D2, D3 e AVF) e pseudo r' na derivação V1. Já nas taquicardias
atrioventriculares, a freqüência cardíaca costuma ultrapassar os 200 bpm, as
ondas P podem estar visíveis, com intervalo RP' mais longo (> a 120 ms),
com ondas P negativas na derivação D1 (se forem vias laterais esquerdas),
infradesnivelamentos do segmento ST e/ou alternância de amplitude do QRS.
O uso inicial das manobras vagais e da adenosina por via
endovenosa em todos os pacientes com taquicardia paroxística supraventricular
estável continua a ser o tratamento de escolha. As novas recomendações incluem o
uso opcional de drogas classe IIb e estratégias de tratamento que possam ser
modificadas pela presença de insuficiência cardíaca congestiva. Com relação ao
uso da adenosina, essa droga é eficaz na reversão da maioria das taquicardias
supraventriculares reentrantes que envolvam a participação do nó
atrioventricular. No entanto, se o nó atrioventricular não participar do
mecanismo de reentrada (como, por exemplo, "flutter" atrial, fibrilação atrial,
taquicardia atrial e taquicardias ventriculares), a adenosina não reverterá
essas arritmias; porém, ao produzir bloqueio atrioventricular, irá facilitar o
diagnóstico correto da arritmia. A dose é semelhante à indicada no tratamento
das taquicardias com QRS largo de origem supraventricular. Quando não se
consegue discriminar uma taquicardia ventricular de uma taquicardia paroxística
supraventricular com aberrância de condução com estabilidade hemodinâmica, não
se tem recomendado o uso rotineiro da adenosina para o diagnóstico diferencial.
A adenosina deve ser usada somente quando a origem supraventricular for
fortemente suspeitada. A adenosina pode causar broncospasmo, devendo ser evitada
em pacientes com pneumopatia. Os pacientes com denervação cardíaca após o
transplante cardíaco podem apresentar hipersensibilidade aos efeitos
bradicárdicos da adenosina. Nos pacientes em uso de derivados da metilxantina
(como, por exemplo, teofilina), a adenosina pode ter sua eficácia reduzida.
Em pacientes com função ventricular esquerda preservada, os
bloqueadores dos canais de cálcio (verapamil e diltiazem) e os betabloqueadores
(metoprolol, esmolol, propranolol) continuam sendo drogas de opção terapêutica
das taquicardias paroxísticas supraventriculares. Quando não se consegue
reversão com as manobras vagais, adenosina ou agentes bloqueadores do nó
atrioventricular, outras opções de drogas antiarrítmicas parenterais podem ser
utilizadas, como procainamida, amiodarona, propafenona, sotalol e flecainida.
Se houver disfunção ventricular esquerda, muita precaução
deve ser tomada, evitando-se drogas com potencial inotrópico negativo, como os
betabloqueadroes, o verapamil, a procainamida, a propafenona, a flecainida e o
sotalol. Nesse caso, são mais recomendáveis o digital por via endovenosa, a
amiodarona e o diltiazem.
Em resumo, na ausência de contra-indicações, as primeiras
medidas a serem tomadas na presença de taquicardia paroxística supraventricular
são as manobras vagais e o uso de adenosina. Se a função ventricular esquerda
for preservada, opções adicionais recomendadas são bloqueadores dos canais de
cálcio (verapamil ou diltiazem — classe I), betabloqueadores (classe I) ou
digital (classe IIb). Quando essas opções são ineficazes, deve-se considerar
fortemente a indicação de cardioversão elétrica. Quando a cardioversão elétrica
não é possível, desejável ou ineficaz, pode-se optar por amiodarona (classe
IIa), procainamida (classe IIa), flecainida (classe IIa), propafenona (classe
IIa) e sotalol (classe IIa). Deve-se salientar que o uso destas últimas drogas
deve ser parenteral rápido e não de "manutenção", pois os riscos de pró-arritmia
aumentam consideravelmente. O uso seriado ou combinado de bloqueadores de canais
de cálcio, betabloqueadores e outros agentes antiarrítmicos também deve ser
desencorajado. Em portadores de insuficiência cardíaca, as drogas recomendadas
são a amiodarona (classe IIb), o digital IV (classe IIb) e o diltiazem (classe
IIb). Nesses pacientes, a cardioversão elétrica deve ser encorajada (classe I).
TAQUICARDIAS ATRIAIS
As taquicardias atriais podem resultar dos três mecanismos:
reentrada, automatismo anormal e atividade deflagrada por pós-potenciais tardios
(intoxicação digitálica). Podem originar-se de um único foco ou de múltiplos
focos (taquicardia atrial multifocal). As taquicardias atriais automáticas
ocorrem freqüentemente em pacientes mais jovens e são distinguidas das formas
reentrantes pelo fato de apresentarem início gradual (fenômeno de "warm up") e
término também gradativo ("cool down"). As manobras vagais e o uso de adenosina
podem demonstrar o bloqueio atrioventricular com a persistência da arritmia
atrial, especialmente nas formas automáticas. Os ritmos automáticos (taquicardia
atrial, taquicardia atrial multifocal, taquicardia sinusal), diferentemente das
arritmias reentrantes, costumam ser irresponsivos à cardioversão elétrica. No
caso das taquicardias atriais multifocais, a causa mais comum é a doença
pulmonar obstrutiva cônica descompensada, devendo-se priorizar o tratamento da
doença de base. Em pacientes com função ventricular esquerda preservada,
recomenda-se o uso de betabloqueadores ou bloqueadores dos canais de cálcio (diltiazem
ou verapamil), que podem proporcionar controle da resposta ventricular ou até
mesmo reversão. Outras drogas úteis podem ser a amiodarona, a flecainida e a
propafenona.
Em resumo, a cardioversão elétrica sincronizada é ineficaz
para o tratamento das taquicardias atriais automáticas (classe III). Nos
pacientes com função ventricular esquerda preservada, podem-se indicar os
bloqueadores dos canais de cálcio (diltiazem ou verapamil — classe IIb), os
betabloqueadores (classe IIb), o digital (classe indeterminada), a amiodarona
(classe IIb), a flecainida IV (classe IIb) e a propafenona por via intravenosa (clase
IIb).
FIBRILAÇÃO ATRIAL E "FLUTTER" ATRIAL
A conduta emergencial da fibrilação atrial e do "flutter"
atrial sofreu modificações significativas. As recomendações passaram a ser mais
específicas, devendo-se ter como considerações iniciais o controle farmacológico
da freqüência cardíaca, o controle farmacológico do ritmo cardíaco, os consensos
sobre o uso da anticoagulação, a presença de vias anômalas (síndrome de
Wolff-Parkinson-White) e as abordagens frente a pacientes com disfunção
ventricular. As causas reversíveis de fibrilação atrial devem, se possível, ser
corrigidas, tais como: hipoxemia, tireotoxicose, anemia, hipertensão,
insuficiência cardíaca congestiva, isquemia coronariana, hipocalemia,
hipomagnesemia e outras condições tóxico-metabólicas. Deve-se, também, destacar
a probabilidade de reversão espontânea da fibrilação atrial aguda. Danias e
colaboradores(46) constataram, em estudo prospectivo, que apenas a
redução da resposta ventricular (com betabloqueadores, digital, verapamil ou
diltiazem), em pacientes hemodinamicamente estáveis, resultou em taxa de
reversão espontânea em torno de 70%, se a fibrilação atrial tinha menos de 24
horas de aparecimento.
Outro tópico importante é a indicação da anticoagulação.
Weigner e colaboradores(47), em estudo prospectivo com 1.822
pacientes, corroboraram a evidência de que se a fibrilação atrial tiver duração
clinicamente estimada abaixo de 48 horas, o risco de fenômeno tromboembólico
relacionado com o procedimento de cardioversão química ou elétrica é
extremamente baixo, tornando desnecessária a anticoagulação profilática. Por
outro lado, se a duração da fibrilação atrial for superior a 48 horas, o risco
de fenômeno tromboembólico após a reversão ao ritmo sinusal irá persistir até
pelo menos três semanas. O uso de antiarrítmicos e a cardioversão elétrica devem
ser evitados, exceto se houver instabilidade hemodinâmica e resposta ventricular
muito rápida. Em pacientes "limítrofes", pode-se tentar a opção de cardioversão
precoce, por meio de heparinização plena por 24 horas e ecocardiograma
transesofágico para excluir a presença de trombos. Nos pacientes com "flutter"
atrial, as recomendações são as mesmas que as da fibrilação atrial, visto que
esta arritmia também tem risco potencial de fenômeno tromboembólico,
especialmente nos portadores de cardiopatia estrutural.
Para o controle da resposta ventricular, enquanto se planeja
a reversão ao ritmo sinusal, pode-se optar por diltiazem por via endovenosa,
verapamil por via endovenosa e betabloqueadores por via endovenosa. A adenosina,
em decorrência de sua curta duração, não é uma droga apropriada para essa
situação. O digital por via endovenosa também pode ser uma opção; porém, por
causa de seu lento início de ação e de sua inatividade frente a estados
hiperadrenérgicos (como, por exemplo, insuficiência cardíaca congestiva), deve
ter seu uso postergado. Na presença de insuficiência cardíaca, os efeitos
inotrópicos negativos são menos pronunciados com o uso do diltiazem, que é
superior ao verapamil e ao betabloqueador(48, 49). A dose inicial de
ataque do diltiazem é de 0,25 mg/kg, em 2 minutos, podendo-se repetir após 15
minutos, com dose superior a 0,35 mg/kg. A dose média de manutenção (se
indicada) é de 10 mg/h, por até 24 horas. Outra opção na vigência de
insuficiência cardíaca congestiva é a amiodarona por via endovenosa,
especialmente nos pacientes refratários(50) ao controle da resposta
ventricular com os agentes farmacológicos já descritos. O risco hipotético de
fenômeno tromboembólico em caso de possível reversão com a amiodarona, nesses
pacientes mais críticos, não se confirmou nos estudos.(51-53)
Outra possibilidade com grande risco de instabilidade
hemodinâmica seria a fibrilação atrial ou "flutter" atrial, com condução
anterógrada por uma via acessória. O diagnóstico é estabelecido pela presença de
fibrilação atrial de alta resposta ventricular, geralmente com freqüências
ventriculares acima de 250 bpm e alternância da duração do QRS, simulando,
muitas vezes, taquicardia ventricular não-sustentada polimórfica. Nessa situação
particular, estão contra-indicadas drogas que possam facilitar a condução pela
via acessória, tais como digital, verapamil, diltiazem e betabloqueadores. Caso
haja a possibilidade de se tratar com drogas, deve-se optar por procainamida,
amiodarona, flecainida ou propafenona, administradas por via endovenosa.
Em resumo, em virtude das considerações descritas, a
cardioversão elétrica sincronizada (classe I) deve ser o tratamento de escolha
para a reversão ao ritmo sinusal da fibrilação atrial ou do "flutter" atrial.
Nos pacientes hemodinamicamente instáveis, é a opção mais segura,
independentemente da duração da fibrilação atrial ou do "flutter". Nos casos com
estabilidade hemodinâmica, deve-se proceder ao controle da resposta ventricular
antes da cardioversão elétrica. É importante frisar a possibilidade de reversão
espontânea enquanto se prepara para a cardioversão. As drogas mais indicadas são
diltiazem (classe I), verapamil (classe I), betabloqueadores (classe I) ou
digital (classe IIb). A adenosina é inapropriada para essa situação (classe
III). Em pacientes com insuficiência cardíaca congestiva, as opções são
diltiazem (classe IIb), digital (classe IIb) e amiodarona (classe IIb). Nos
casos de presença concomitante de condução por uma via acessória, estão
contra-indicados digital (classe III), betabloqueadores (classe III) e
bloqueadores de cálcio (classe III). Está indicada a cardioversão elétrica
sincronizada (classe I). Se a cardioversão elétrica não puder ser feita, se não
for bem-sucedida ou se não for escolhida, pode-se optar por procainamida (classe
IIb), propafenona (classe IIb), amiodarona (classe IIb), flecainida (classe IIb)
ou sotalol por via endovenosa (classe IIb). Se houver a concomitância de
fibrilação atrial, insuficiência cardíaca congestiva e síndrome de
Wolff-ParkinsonWhite, só se justifica o uso de amiodarona (classe IIb). Se for
indicada a reversão farmacológica nos pacientes com fibrilação atrial com menos
de 48 horas de duração e sem cardiopatia estrutural ou vias anômalas, cuja
cardioversão elétrica sincronizada seja ineficaz, impossível ou não escolhida,
pode ser utilizado um arsenal de drogas antiarrítmicas para administração
endovenosa, já testadas na literatura (apenas uma delas): amiodarona (classe
IIa), ibutilida (classe IIa), propafenona (classe IIa), procainamida (classe
IIa), flecainida (classe IIa), sotalol (classe IIb) e procainamida (classe IIb).
Como lembretes finais, todos os esforços devem ser feitos
para minimizar o risco de fenômeno tromboembólico, incluindo a anticoagulação em
todos os casos com duração superior a 48 horas. Nessas situações, controla-se a
resposta ventricular com verapamil, diltiazem ou betabloqueadores
(alternativamente, a amiodarona, para os casos mais "difíceis"); inicia-se a
anticoagulação oral com controles de INR estáveis por pelo menos três semanas,
mantendo-se a anticoagulação por mais três a quatro semanas após a reversão ao
ritmo sinusal.
A cardioversão elétrica sincronizada deve ser o tratamento de
escolha para a reversão ao ritmo sinusal. A energia recomendada é de 100 J a 200
J na fibrilação atrial, e de 50 J a 100 J no "flutter" atrial. A quantidade do
número de choques e a seqüência dos mesmos ainda é controversa, aguardando-se
estudos mais abrangentes.
TAQUICARDIA JUNCIONAL
Esta é uma forma rara de arritmia em adultos, geralmente
causada por automatismo anormal e/ou atividade deflagrada. Pode ocorrer em
alguns casos de intoxicação digitálica (mais bem tratada com a suspensão da
droga) e de intoxicação por drogas vasoativas ou teofilina (mais bem tratadas
com redução ou suspensão da infusão da droga) ou no pós-operatório de cirurgias
congênitas. A taquicardia juncional "pura" é muito rara. Nos casos sintomáticos,
as recomendações, não baseadas em fortes evidências, seriam o uso de amiodarona
por via endovenosa (classe IIb) ou de betabloqueadores (classe indeterminada) ou
bloqueadores de cálcio (classe indeterminada).
OUTROS AGENTES ANTIARRÍTMICOS
Algumas intervenções diante de arritmia emergencial podem
necessitar de agentes farmacológicos que não necessariamente se enquadram na
classificação padronizada das drogas antiarrítmicas. Esses agentes
farmacológicos serão aqui citados, bem como algumas drogas antiarrítmicas.
Atropina
A principal indicação da atropina é no tratamento da
bradicardia sinusal sintomática (classe I), podendo também ser benéfica nos
bloquei-os atrioventriculares nodais (classe IIa) ou nas assistolias
ventriculares. Não está indicada nos casos de bloqueios atrioventriculares
infranodais (Mobitz II), pois não haverá resposta terapêutica. Nos raros casos
de ritmo idioventricular acelerado com instabilidade hemodinâmica, a atropina
também pode ser útil. Essa droga deve ser utilizada com cautela na vigência de
infarto agudo do miocárdio, pois o aumento súbito da freqüência cardíaca pode
piorar a isquemia ou aumentar a zona de infarto. Raramente ocorre fibrilação
ventricular ou taquicardia ventricular após a administração da droga. A dose
recomendada do sulfato de atropina na assistolia e na atividade elétrica sem
pulso é de 1,0 mg por via endovenosa, repetida a cada 3 a 5 minutos se a
assistolia persistir. Para a bradicardia, a dose recomendada é de 0,5 mg a 1,0
mg por via endovenosa a cada 3 a 5 minutos, numa dose total de 0,04 mg/kg.
Isoproterenol
O isoproterenol está recomendado como medida temporária
enquanto se implanta o marcapasso provisório na taquicardia ventricular
polimórfica por "torsades de pointes" (classe indeterminada). Também está
indicado para o rápido controle de bradicardia com instabilidade hemodinâmica,
quando não ocorre resposta à atropina e à dopamina e o marcapasso provisório não
se encontra disponível (classe IIb). A droga deve ser administrada somente em
baixas doses, pois altas doses estão relacionadas com aumento do consumo de
miocárdio, aumento da área infartada e arritmias ventriculares malignas. O
isoproterenol está contra-indicado em pacientes em parada cardíaca. A dose
recomendada é de 2 µg/min a 10 µg/min em infusão com solução salina (1 mg + 500
ml de solução fisiológica = 2 µg/ml), titulando-se conforme a freqüência
cardíaca e o ritmo cardíaco. Todas as evidências do tratamento com isoproterenol
são limitadas.
Sulfato de magnésio
A hipomagnesemia pode causar fibrilação ventricular
refratária e pode mascarar a hipopotassemia intracelular. A deficiência de
magnésio deve ser corrigida assim que diagnosticada. Em situações de emergência,
o sulfato de magnésio é administrado na dose de 1 g a 2 g por via endovenosa,
diluídos em 100 ml de solução glicosada, por um a dois minutos. A infusão mais
rápida pode ocasionar hipotensão e até assistolia. Experiências anedóticas
sugerem o benefício do magnésio na "torsades de pointes" decorrente de QT longo
adquirido por drogas, pois estabilizaria a dispersão da repolarização, abolindo
a atividade deflagrada por pós-potenciais. Após a dose de ataque, pode-se manter
uma dose de 0,5 g a 1,0 g (4 mEq a 8 mEq) por hora. O uso profilático do sulfato
de magnésio em pacientes com infarto do miocárdio não encontra respaldo atual na
literatura médica.
Dopamina
Os efeitos beta-agonistas da dopamina são menos pronunciados
que os do isoproterenol. Por ser um agente mais seguro, tem preferência sobre o
isoproterenol para as bradicardias refratárias ou com contra-indicação à
atropina. A dose inicial recomendada é de 3,0 µg/kg/min a 7,5 µg/kg/min. O uso
da dopamina como agente vasodilatador renal na insuficiência renal oligúrica não
está mais indicado.(54)
Bretílio
O tosilato de bretílio foi retirado dos algoritmos na última
diretriz do ACLS por causa da alta ocorrência de efeitos colaterais, do pequeno
suprimento industrial, pelo pouco uso, e da preferência por outros agentes
farmacológicos mais seguros. Era utilizado nas taquicardias ventriculares ou nas
fibrilações ventriculares não-responsivas à desfibrilação e à adrenalina.
Ibutilida
A ibutilida é um antiarrítmico "puro" de classe III,
disponível apenas na forma parenteral. A principal característica da droga é sua
capacidade de atuar em arritmias atriais com ciclos de freqüência estáveis e
mais lentos, como no "flutter" atrial (efeito "reverso-dependente)(55).
Pode ser uma opção interessante na tentativa de reversão do "flutter" atrial,
quando não se deseja a cardioversão elétrica. Em recente publicação(56),
a taxa de reversão do "flutter" atrial ao ritmo sinusal com o uso da ibutilida
situou-se em torno de 50%. Também pode ser efetiva na reversão da fibrilação
atrial, especialmente como droga adjunta nas formas persistentes e refratárias à
cardioversão elétrica inicial(57). No entanto, em decorrência de sua
curta duração de ação, a ibutilida pode ser menos efetiva na manutenção do ritmo
sinusal. Além disso, a droga deve ser evitada em pacientes com disfunção
ventricular, por causa do potencial de pró-arritmia, incluindo "torsades de
pointes" (em torno de 4,4%)(58). Seu uso deve ser feito com
monitorização cardíaca contínua, mesmo após o término da infusão, por 4 a 6
horas. A dose recomendada para adultos com mais de 60 kg de peso corporal é de 1
mg (10 ml) por via endovenosa, diluído ou não, por 10 minutos, podendo ser
repetida 10 minutos após, se necessário. Em pacientes com menos de 60 kg, a dose
é de 0,01 mg/kg. Até o fechamento desta edição, a ibutilida ainda não estava
disponível, no Brasil, para uso comercial.
CONCLUSÃO
Em resumo, os agentes farmacológicos utilizados nas arritmias
cardíacas emergenciais possuem sua indicação conforme a situação clínica do
paciente, o ritmo cardíaco de base e a seqüência de eventos durante as medidas
de tratamento iniciais. A Tabela 1 ilustra, resumidamente, essas indicações,
conforme as evidências atuais (classes I, IIa, IIb, III e indeterminada),
considerando-se apenas as drogas disponíveis no Brasil.
| Tabela 1. Cenário atual dos principais
agentes farmacológicos frente às arritmias cardíacas, de acordo com o ACLS
Internacional(2). |
| |
Classe
|
|
Droga
|
I
|
IIa
|
IIb
|
III
|
Indeterminada
|
Lidocaína
Adenosina
Adrenalina
Atropina
Isoproterenol
Dopamina
Magnésio
Procainamida
Bloqueador de cálcio
Beta- bloqueador
Propafenona
Amiodarona
Digital IV |
TPSV estáveis
- AESP após CVE - Assistolia
Brad. sinusal sintomática
Hipomagnesemia comprovada
TPSV estável FA < 48 h, antes
CVE TPSV estável FA < 48 h, antes CVE
|
BAV 2o grau hissiano
Brad. sinusal refratária
TPSV TV estável FA / “flutter”
FA < 48 h s/ ICC
- TPSV estável s/ ICC
- FA < 48 h
|
TV estável
Brad. sinusal refratária
FA + WPW Taq. QRS largo
FA > 48 h + ICC (diltiazem)
FA < 48 h + WPW
- TPSV estável c/ ICC
- TV estável
- TV/FV refratária
- TV polimórfica + QT NL.
- FA + WPW
- FA > 48 h + ICC - TPSV estável
|
FA + WPW
BAV 2o grau hissiano
- PCR - Hipotensão - TV/FV
Profilático no IAM
FA + WPW TPSV + ICC
TPSV ou FA + ICC FA + WPW
TV polimórfica + QT longo
FA + WPW
|
- AESP (1) refratária - IAM + EV freq.+ ID (2)
“Torsades de pointes”, antes do MPP
Profilático no IAM
|
|
AESP = atividade elétrica sem pulso; BAV = boqueio atrioventricular; Brad.
= bradicardia; CVE = cardioversão elétrica; FA = fibrilação atrial; FV =
fibrilação ventricular; IAM = infarto agudo do miocárdio; ICC =
insuficiência cardíaca congestiva; ID = indisponibilidade do desfibrilador;
MPP = marcapasso provisório; PCR = parada cardiorrespiratória; TPSV =
taquicardias paroxísticas supraventriculares; TV = taquicardia
ventricular; WPW = síndrome de Wolff-Parkinson-White.
|
REFERÊNCIAS
1. American Heart Association. Guidelines for Cardiopulmonary
Resuscitation Emergency Cardiac Care. JAMA 1992;268:2212-302.
2. Guidelines for Cardiopulmonary Resuscitation and Emergency
Cardio-Vascular Care. Circulation 2000;102(8):1-384.
3. Schnittger I, Rodriguez IM, Winkle RA. Esophageal
electrocardiography: a new technology revives an old technique. Am J Cardiol
1986;57:601-7.
4. Stewart RB, Bardy GH, Greene HL. Wide complex tachycardia:
misdiagnosis and outcome after emergent therapy. Ann Intern Med 1986;104:766-71.
5. Akhtar M, Shenasa M, Jazayeri M, Caceres J, Tchou PJ. Wide
QRS complex tachycardia: reappraisal of a common clinical problem. Ann Intern
Med 1988;109:905-12.
6. Brugada P, Brugada J, Mont L, Smeets J, Andries EW. A new
approach to the differential diagnosis of a regular tachycardia with a wide QRS
complex. Circulation 1991;83:1649-59.
7. Antunes E, Brugada J, Steurer G, Andries E, Brugada P. The
differential diagnosis of a regular tachycardia with a wide QRS complex on the
12-lead ECG: ventricular tachycardia, supraventricular tachycardia with aberrant
intraventricular conduction, and supraventricular tachycardia with anterograde
conduction over an accessory pathway. Pac Clin Electrophysiol 1994;17:1515-24.
8. Steurer G, Gursoy S, Frey B, Simonis F, Andries E, Kuck K,
et al. The differential diagnosis on the electrocardiogram between ventricular
tachycardia and preexcited tachycardia. Clin Cardiol 1994;17:306-8.
9. Wellens HJ, Bar FW, Lie KI. The value of the
electrocardiogram in the differential diagnosis of a tachycardia with a widened
QRS complex. Am J Med 1978;64:27-33.
10. Kindwall KE, Brown J, Josephson ME. Electrocardiographic
criteria for ventricular tachycardia in wide complex left bundle branch block
morphology tachycardias. Am J Cardiol 1988;61:1279-83.
11. Herbert ME, Votey SR, Morgan MT, Cameron P, Dziukas L.
Failure to agree on the electrocardiographic diagnosis of ventricular
tachycardia. Ann Emerg Med 1996;27:35-8.
12. Littmann L, McCall MM. Ventricular tachycardia may
masquerade a supraventricular tachycardia in patients with preexisting
bundle-branch block. Ann Emerg Med 1995;26:98-101.
13. Halperin BD, Kron J, Cutler JE, Kudenchuk PJ, McAnulty JH.
Misdiagnosing ventricular tachycardia in patients with underlying conduction
disease and similar sinus and tachycardia morphologies. West J Med 1990;152:
677-82.
14. Lerman BB, Bernardinelli L, West G, et al.
Adenosine-sensitive ventricular tachycardia: evidence suggesting cyclic
AMP-mediated triggered activity. Circulation 1986;74:270-80.
15. Lerman BB, Stein KM, Markowitz SM. Mechanism of
idiopathic left ventricular tachycardia. J Cardiovasc Electrophysiol 1997;
8(5):571-83.
16. Armengol RE, Graff J, Baerman JM, Swiryn S. Lack of
effectiveness of lidocaine for sustained, wide QRS tachycardia. Ann Emerg Med
1989;18:254-7.
17. Nasir Jr N, Taylor A, Doyle TK, Pacifico. An evaluation
of intravenous lidocaine for the termination of sustained monomorphic
ventricular tachycardia in patients with coronary artery disease with or without
healed myocardium infarction. Am J Cardiol 1994;74: 1183-6.
18. Gorgels AP, van den Dool A, Hofs A, et al. Comparison of
procainamide and lidocaine in terminating sustained monomorphic ventricular
tachycardia. Am J Cardiol 1996;18:43-6.
19. Ho DS, Zecchim RP, Richards DA, Uther JB, Ross DL.
Double-blind trial of lidocaine versus sotalol for acute termination of
spontaneous sustained ventricular tachycardia. Lancet 1994;344:18-23.
20. Alexander JH, Granger CB, Sadowski Z, et al. The GUSTO-I
and GUSTO-IIb Investigators. Prophylatic lidocaine use in the acute myocardium
infarction: incidence and outcomes from two international trials. Am Heart J
1999;137:799-805.
21. Garrat CJ, Griffith MJ, O'Nunaim S, Ward D, Camm AJ.
Effects of intravenous adenosine on antegrade refractoriness of accessory
atrio-ventricular connections. Circulation 1991;84:1962-8.
22. Brodsky MA, Hwang C, Hunter D, et al. Life-threatening
alterations in heart rate after the use of adenosine in atrial flutter. Am Heart
J 1995;130:564-71.
23. Sharma AD, Klein GJ, Yee R. Intravenous adenosine
triphosphate during wide QRS complex tachycardia: safety, therapeutic efficacy,
and diagnostic utility. Am J Med 1990;88:337-43.
24. Callans DJ, Marchlinski FE. Dissociation of termination
and prevention of inducibility of sustained ventricular tachycardia with fusion
of procainamide: evidence for distinct mechanisms. J Am Coll Cardiol
1992;19:111-7.
25. Leitch JW, Klein GJ, Yee R, Feldman RD, Brown J.
Differential effect of intravenous procainamide on anterograde and retrograde
accessory pathway refractoriness. J Am Coll Cardiol 1992;19:118-24.
26. Wellens HJ, Braat S, Brugada P, Gorgels AP, Bar FW. Use
of procainamide in patients with the Wolff-Parkinson-White syndrome to disclose
a short refractory period of the accessory pathway. Am J Cardiol 1982;50:1087-9.
27. Burkart F, Pfisterer M, Kiowski W, Follath F, Burckardt
D. Effect of anti-arrhythmic therapy on mortality in survivors of myocardium
infarction with asymptomatic complex ventricular arrhythmias. Basel
Antiarrhythmic Study of Infarct Survival (BASIS). J Am Coll Cardiol
1990;72:1243-8.
28. Doval HC, Nul DR, Grancelli HO, Perrone SV, Bortman GR,
Curiel R, for Grupo de Estudio de le Sobrevida en la Insuficiencia Cardiaca en
Argentina (GESICA). Randomised trial of low-dose amiodarone in severe congestive
heart failure. Lancet 1994;344:493-8.
29. Cairns JA, Connolly SJ, Roberts RS, Gent M, and the
CAMIAT Investigators. Randomized trial of outcome after myocardial infarction in
patients with frequent or repetitive ventricular premature depolarizations:
CAMIAT. Lancet 1997;349:675-82.
30. Julian DG, Camm AJ, Frangin G, et al. EMIAT Investigators.
Randomized trial of effect of amiodarone on mortality in patients with left
ventricular dysfunction after recent myocardial infarction: EMIAT. Lancet 1997;
349:667-74.
31. Amiodarone Trials Meta-Analysis Investigators. Effect of
prophylatic amiodarone on mortality after acute myocardial infarction and in
congestive heart failure: meta-analysis of individual data from 6,500 patients
in randomized trials. Lancet 1997;350:1417-24.
32. Leak D. Intravenous amiodarone in the treatment of
refractory life-threatening cardiac arrhythmias in the critically ill patient.
Am Heart J 1986;11:456-62.
33. Moss NA, Mohiuddin SM, Hee TT, et al. Efficacy and
tolerance of high-dose intravenous amiodarone for recurrent, refractory
ventricular tachycardia. Am J Cardiol 1990;65:609-14.
34. Schutzenberger W, Leisch F, Kerschner K, Harringer W,
Herbinger W. Clinical efficacy of intravenous amiodarone in the short term
treatment of recurrent sustained ventricular tachycardia and ventricular
fibrillation. Br Heart J 1989;62:367-71.
35. Levine JH, Massumi A, Scheinman MM, et al. Intravenous
Amiodarone Multicenter Trial Group. Intravenous amiodarone for recurrent
sustained hypotensive ventricular tachyarrhythmias. J Am Coll Cardiol
1996;27:67-75.
36. Scheinman MM, Levine JH, Cannom DS, et al. The
Intravenous Amiodarone Multicenter Investigators Group. Dose-ranging study of
intravenous amiodarone in patients with life-threatening ventricular
tachyarrhythmias. Circulation 1995;92:3264-72.
37. Kudenchuk PJ, Cobb LA, Copass MK, et al. Amiodarone for
resuscitation after out-of-hospital cardiac arrest due to ventricular
fibrillation. N Engl J Med 1999;341:871-8.
38. Remme WJ, Kruyssen HA, Look MP, van Hoogenhuyze DC,
Krauss XH. Hemodynamic effects and tolerability of intravenous amiodarone in
patients with impaired left ventricular function. Am Heart J 1991;122:96-103.
39. Totterman KJ, Turto H, Pellinen T. Overdrive pacing as a
treatment of sotalol-induced ventricular tachyarrhythmias (torsades de pointes).
Acta Med Scand Suppl 1982;668:28-33.
40. Inoue H, Matsuo H, Mashima S, Murao S. Effects of atrial
pacing, isoprenaline and lidocaine on experimental polymorphous ventricular
tachycardia. Cardiovasc Res 1984; 18:538-47.
41. Borer JS, Harrison LA, Kent KM, Levy R, Goldstein RE,
Epstein SE. Beneficial effect of lidocaine on ventricular electrical stability
and spontaneous ventricular fibrillation during experimental myocardium
infarction. Am J Cardiol 1976;37:860-3.
42. Kowey PR. An overview of antiarrhythmic drug management
of electrical storm. Can J Cardiol 1996;12(suppl B):3B-8B.
43. Kudenchuk PD, Cobb L, Fahrenbruch C, et al. The ARREST
Trial. Randomized controlled trial of amiodarone versus placebo in the early
treatment of refractory VF arrest in the out-of-hospital setting. Circulation
1997;96.
44. Kentsch M, Berkel H, Bleifeld W. Intravenous
amiodaron-applikattion bei therapierefraktarem kammerflimmem. Intensivmedizin
1988; 25:70-4.
45. Weaver WD, Fahrenbruch CE, Johnson DD, Hallstrom AP, Cobb
LA, Copass MK. Effect of epinephrine and lidocaine therapy on outcome after
cardiac arrest due to ventricular fibrillation. Circulation 1990;82:2027-34.
46. Danias PG, Caufield TA, Weigner MJ, Silverman DI, Manning
WJ. Likelihood of spontaneous conversion of atrial fibrillation to sinus rhythm.
J Am Coll Cardiol 1998;31:588-92.
47. Weigner MJ, Caufield TA, Danias PG, Silverman DI, Manning
WJ. Risk for clinical thromboembolism associated with conversion to sinus rhythm
in patients with atrial fibrillation lasting less than 48 hours. Ann Intern Med
1997;126:615-20.
48. Goldenberg IF, Lewis WR, Dias VC, Heywood JT, Pedersen WR.
Intra-venous diltiazem for the treatment of patients with atrial fibrillation or
flutter and moderate to severe congestive heart failure. Am J Cardiol
1994;74:884-9.
49. Heywood JT, Graham B, Marias GE, Jutzt KR. Effects of
intravenous diltiazem on rapid atrial fibrillation accompanied by congestive
heart failure. Am J Cardiol 1991;67:1150-2.
50. Clemo HF, Wood WA, Gilligan DM, Ellenbogen KA.
Intravenous amiodarone for acute heart rate control in the critically ill
patient with atrial tachyarrhythmias. Am J Cardiol 1998;81:594-8.
51. Cotter G, Blatt A, Kaluski E, et al. Conversion of recent
onset paroxysmal atrial fibrillation to normal sinus rhythm: the effect of no
treatment and high-dose amiodarone: a randomized, placebo-controlled study. Eur
Heart J 1999;20:1833-42.
52. Kerin NZ, Faitel K, Naini M. The efficacy of intravenous
amiodarone for the conversion of chronic atrial fibrillation: amiodarone vs
quinidine for conversion of atrial fibrillation. Arch Intern Med 1996;156:49-53.
53. Hou ZY, Chang MS, Chen CY, et al. Acute treatment of
recent-onset atrial fibrillation and flutter with a tailored dosing regimen of
intravenous amiodarone: a randomized, digoxin-controlled study. Eur Heart J
1995;16:521-8.
54. Chertow GM, Sayegh MH, Allgren RL, Lazarus JM. Auriculin
Anaritide Acute Renal Failure Study Group. Is the administration of dopamine
associated with adverse or favorable outcomes in acute renal failure? Am J Med
1996;101:49-53.
55. Buchanan LV, Turcotte UM, Kabell GC, et al.
Antiarrhythmic and electrophysiologic effects of ibutilide in a chronic canine
model of atrial flutter. J Cardiovasc Pharmacol 1993;22:10-4.
56. Ellenbogen KA, Stamber BS, Wood MA. Efficacy of
intravenous ibutilide for rapid termination of atrial fibrillation or flutter: a
dose-response study. J Am Coll Cardiol 1996;28: 130-6.
57. Oral H, Souza JJ, Michaud GF. Facilitating transthoracic
cardioversion of atrial fibrillation with ibutilide pretreatment. N Engl J Med
1999;340:1849-54.
58. Kowey PR, Vander Lugt JT, Luderer JR. Safety and risk/benefit
analysis of ibutilide for acute conversion of atrial fibrillation/flutter. Am J
Cardiol 1996;78:46-52.
FRANCISCO DARRIEUX, FLÁVIO TARASOUTCHI
