 Dr. Donald Ross
Dr. Donald RossAutoenxerto pulmonar para Doença Valvar Aórtica (Cirurgia de Ross)
 Dr. Donald Ross
Dr. Donald Ross
Veja o vídeo da Cirurgia de Ross
1. Introdução
Em 1967, Donald Ross descreveu uma técnica cirúrgica indicada para pacientes com necessidade de troca valvar aórtica, que consiste na substituição da valva aórtica doente pela valva pulmonar do próprio paciente ("autoenxerto") na posição aórtica, enquanto a valva pulmonar retirada é substituída por uma prótese biológica, um homoenxerto aórtico ou pulmonar. Inicialmente chegou-se a utilizar outras próteses biológicas com resultados pobres.
Desde o desenvolvimento inicial das técnicas cirúrgicas para troca valvar aórtica, existe a questão da prótese aórtica ideal. As próteses mecânicas apresentam excelente durabilidade, porém, com características hemodinâmicas subótimas e necessidade de anticoagulação. As próteses biológicas, mesmo homoenxertos, têm durabilidade limitada.
Acreditava-se que, devido a sua grande similaridade estrutural com a valva aórtica, sua viabilidade e o fato de ser autólogo, a valva pulmonar seria o substituto ideal para valva aórtica, sobretudo em jovens; podendo ser o autoenxerto pulmonar a opção mais fisiológica quando existe a necessidade de uma prótese que permaneça por toda uma vida.
O autoenxerto apresenta excelente durabilidade. A calcificação valvar não é observada e a degeneração histológica é rara. Como permanece viável, tem o potencial de reparar o dano celular e crescer. Essas características a tornam opção teoricamente mais adequada para pacientes jovens.
As dúvidas são basicamente três: 1) se a valva pulmonar e o fragmento de artéria pulmonar que são implantados na posição aórtica resistem às altas pressões aórticas; 2) a cirurgia é uma dupla troca valvar, existindo duas próteses em risco e 3) sendo uma dupla troca valvar, é uma cirurgia com tempo de extracorpórea prolongado e muito complexa.
Avaliações de resistência mostram que a valva pulmonar tem força de tensão semelhante à valva aórtica; existem menos estudos com o fragmento (raiz) da artéria pulmonar, porém dilatação excessiva do autoenxerto pulmonar não foram confirmadas em longo prazo. As séries mostram mortalidade operatória em cirurgia do autoenxerto comparáveis as outras cirurgias de troca valvar aórtica.
A reconstrução do trato de saída pulmonar com homoenxerto
pulmonar ou aórtico tem uma chance de 80% de resistir, pelo menos, 16 anos. Em
pacientes com expectativa de vida longa - maior que 40 anos - isto pode
significar uma nova cirurgia cardíaca no futuro, apesar de aparentemente ser uma
cirurgia de excelentes resultados. Existe a necessidade de um seguimento para
avaliação da degeneração do homoenxerto na posição pulmonar.
Apesar de não totalmente determinadas, o autoenxerto pulmonar é a opção que mais se aproxima do normal para substituição valvar aórtica. Apresenta potencial de cura da doença valvar aórtica, fornecendo à criança uma valva que irá crescer a proporção do crescimento somático. Não necessita de anticoagulação e é essencialmente sem risco de tromboembolismo. O estilo de vida do paciente com autoenxerto é o mais próximo do normal dentre as opções das próteses valvares.
O autoenxerto pulmonar é o melhor substituto disponível para valva aórtica em crianças, jovens, mulheres que desejem engravidar e, quase certamente, para pacientes com expectativa de vida maior que 20 anos.
3. Contra-Indicações
São basicamente relacionados a qualidade da valva pulmonar. A presença de regurgitação pulmonar leve e disparidade de diâmetro entre anulo aórtico e pulmonar maior que 2-3 mm contra-indicam esta cirurgia. A presença de ramo conal grande da artéria descendente anterior também é contra-indicação da cirurgia.
A cirurgia consiste de 4 tempos básicos: 1) retirada da valva aórtica doente; 2) inspeção e retirada da valva pulmonar, 3) inserção do valva pulmonar na posição aórtica, 4) inserção de homoenxerto na posição pulmonar.
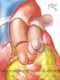
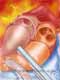
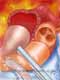

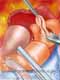
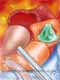
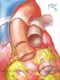
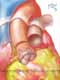
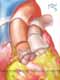

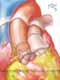
Requer canulação de ambas as cavas e "bypass" cardiopulmonar total. É utilizada cardioplegia retrógrada e anterógrada.
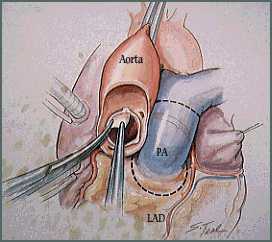
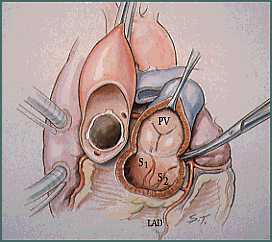
A mobilização da aorta proximal e tronco da artéria pulmonar é realizado após instituição de extracorpórea. Deve-se proceder com a inspeção visual da valva pulmonar. É realizada retirada da valva pulmonar com margens inferior e superior, com inclusão de parte de artéria pulmonar e de pequena quantidade de músculo do ventrículo direito.
O implante do autoenxerto é orientado de modo que o seio pulmonar posterior torna-se o seio não-coronariano. As artérias coronárias são reimplantadas. É implantado homoenxerto (pulmonar preferencialmente) em posição pulmonar. Após o desmame de extracorpórea as competências valvares são avaliadas através de ecocardiograma transesofágico.
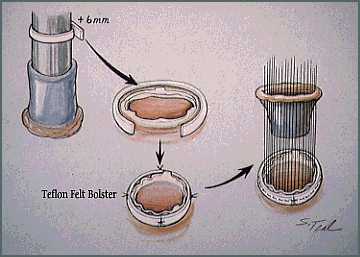
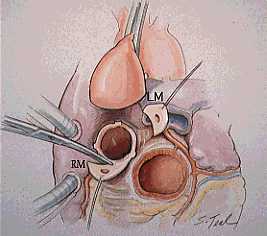
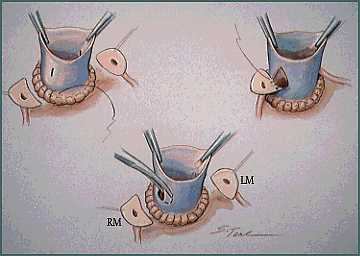
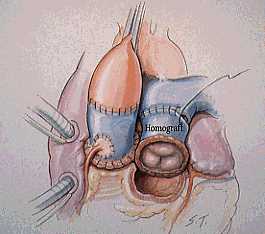
A mortalidade operatória em várias séries foi de aproximadamente de 5%. As técnicas cirúrgicas atuais, por exemplo preservação da primeira artéria septal e manutenção do correto alinhamento das cúspides do autoenxerto, podem ser realizadas com complicações peri-operatórias mínimas e bons resultados. Kouchoukos et al relataram, em 1994, trinta e três pacientes operados sem óbitos e 1 reoperação passados 48 meses.
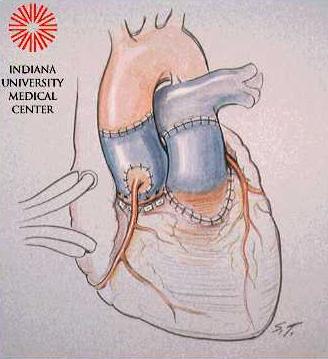
Em 1997 foram publicados os resultados dos pacientes operados pioneiramente por Ross no National Heart Institute, em Londres. Foram avaliados 131 pacientes que obtiveram alta hospitalar operados entre 1967 e 1984.
Neste período foram operados 151 pacientes e seus resultados revistos em 1994. A idade, na cirurgia, era de 11 a 52 anos (média de 32 anos). Predominavam pacientes do sexo masculino (109 pacientes), o tempo médio de extracorpórea foi de 141 minutos (65 - 226 minutos).
Em 113 pacientes foi utilizado homoenxerto para substituir a valva pulmonar. A sobrevida após 10 e 20 anos de cirurgia foi de 85% e 61% respectivamente. Após 10 e 20 anos não houve necessidade de troca do autoenxerto em 88% e 75% dos pacientes e não houve necessidade de troca do homoenxerto em posição pulmonar em 89% e 80%. Causas de óbito incluiam insuficiência cardíaca (12), complicações da reoperação e endocardite.
O motivo mais comum da reoperação foi regurgitação do autoenxerto devido, primordialmente, a problemas técnicos durante o implante (prolapso de cúspide). Nos autoenxertos retirados (30), apenas 3 mostraram sinais de degeneração.
Mortalidade
Em 1994 ocorreram 53 óbitos da série original de 131 pacientes; mortes precoces
(< 1 ano de cirurgia) foram 3 (regurgitação grave do autoenxerto, endocardite no
homoenxerto e morte súbita), 12 óbitos foram complicações de reoperações, quase
todos óbitos devido síndrome de baixo débito pós-operatório e sepse, e 38 óbitos
tardios (causas cardíacas em 29, não cardíaca em 4 e desconhecida em 5).
Regurgitação do autoenxerto foi causa primária de óbito em 14 pacientes (ICC em 8 e reoperações em 6) e endocardite foi em 7 óbitos (4 óbitos em reoperações).
Reoperações
Dos 131 pacientes, 46 foram reoperados num total de 62 reoperações. Não houve necessidade de reoperações em 76% e 62% dos pacientes após, respectivamente, 10 e 20 anos de cirurgia.
Reoperações no autoenxerto
Foram realizadas 35 reoperações no autoenxerto pulmonar, 5 precoces (2 por regurgitação grave, 1 por hemorragia na raiz da aorta, 2 por isquemia miocárdica) e 30 tardias (28 por regurgitação grave, 1 por falso aneurisma de raiz de aorta, 1 por endocardite/abscesso de raiz de aorta). As cirurgias foram a troca valvar (24), reparo do autoenxerto (10) e reparo do falso aneurisma (1)
Dos 30 pacientes submetidos a reoperação por regurgitação do autoenxerto, em 3 esta se apresentou de forma abrupta e grave secundária à endocardite; no restante se apresentou de forma insidiosa durante um período de até 20 anos.
Na reoperação destes pacientes foi observado que as causas da regurgitação eram prolapso das cúspides, avulsão e perfuração.
É importante salientar que em várias destas reoperações do autoenxerto a motivação básica do procedimento cirúrgico foi a troca da prótese em posição pulmonar (geralmente próteses que não eram homoenxerto ou homoenxerto esterilizados por irradiação ou óxido etileno), em que os cirurgiões acharam adequado a troca simultânea do autoenxerto com disfunção moderada.
Não houve necessidade de cirurgias em 10 e 20 anos de acompanhamento em 88% e 75% dos pacientes, respectivamente.
Reoperações na prótese em posição pulmonar
Nos 113 pacientes com homoenxerto na posição pulmonar ocorreram 22 reoperações (2 precoces por infecção e 20 tardias). Nas 20 tardias, 15 por estenose (11 por calcificação e 4 por estenose na linha de sutura), 4 por regurgitação e 1 por dano cirúrgico.
A retenção do homoenxerto em 10 e 20 foi, respectivamente, de 89% e 80%.
Todos os doentes com próteses biológicas que não eram homoenxerto foram submetidos a reoperações ou morreram.
Endocardite e Tromboembolismo
Ocorreram 12 episódios de Endocardite Infecciosa em 12 pacientes; 3 precoces no homoenxerto, presumivelmente infectadas no momento do implante cirúrgico, 4 episódios de endocardite no primeiro ano de reoperação em próteses em posição aórtica (3, não-autoenxertos) e posição mitral (1). Os restantes (5 episódios) foram tardios (de 2 até 15 anos), sendo 1 no homoenxerto em posição mitral, 1 em prótese aórtica e 3 no autoenxerto.
Dezesseis pacientes apresentaram eventos tromboembólicos, 11 sistêmicos e 5 pulmonares. Fatores de risco foram identificados em 15 pacientes: fibrilação atrial, endocardite, doença vascular periférica e insuficiência cardíaca. Um paciente com amaurosis fugax não apresentava outro fator de risco além do que o autoenxerto. Anticoagulação só era administrada na coexistência de fatores de risco.
Avaliação dos sobreviventes
Dentre os 131 pacientes que sobreviveram a cirurgia, 72 estavam vivos, 53 mortos e 6 foram perdidos ao final da série. Dentre os pacientes vivos a média de tempo pós cirúrgico era de 20 anos (10 - 26 anos) com uma classificação NYHA média de 1.2 (1 - 3). Cinqüenta e oito pacientes (81%) mantinham o autoenxerto; a avaliação ecocardiográfica não mostrou estenose, e a maioria (75%) não mostrava regurgitação. Cinqüenta e nove pacientes (82%) mantinham o homoenxerto em posição pulmonar, a maioria sem regurgitação, porém 25 apresentavam algum grau de estenose (gradiente de 20 mmHg).
Nesta série o autoenxerto de valva pulmonar funcionou com notável preservação da viabilidade celular e arquitetura tecidual. A principal causa de reoperação, a regurgitação, se deveu, em sua grande maioria, a problemas técnicos durante o ato cirúrgico, provavelmente devido a um a suspensão inadequada das cúspides no momento do implante valvar.
Um pequeno número de regurgitação foi devido à endocardite, degeneração e alterações reumáticas, o aparente potencial do autoenxerto ser afetado pela doença reumática é descrito; é possível que em locais aonde a doença reumática seja mais comum isto se torne um risco para o implante do autoenxerto (a não ser, talvez, se for mantido a profilaxia com penicilina).
A sobrevida do homoenxerto foi favorável (podem ainda melhorar com o aprimoramento das técnicas de manutenção do homoenxerto); o implante do homoenxerto era e é um dos principais argumentos contrários a cirurgia de Ross.
Se compararmos o resultados desta séria com outras séries de troca valvar aórtica, veremos que as próteses biológicas, em pacientes jovens, têm durabilidade baixa. No Edimburg Heart Valve Trial o percentual dos pacientes com menos de 50 anos que utilizaram biopróteses heteroenxerto livres de reoperação é de 40% após 12 anos de seguimento. Em séries em que se utilizaram homoenxerto o percentual de pacientes livres de reoperação é de 54% após 14 anos.
As próteses mecânicas mostram excelente durabilidade. A grande desvantagem é a necessidade do uso da anticoagulação. No Edimburg Heart Valve Trial mostrou-se uma incidência de 22.5% de eventos hemorrágicas maiores. Além disso, a anticoagulação é um sério incoveniente para pacientes jovens ativos, em pacientes que desejem engravidar e pacientes que necessitem de uso de esteróides ou antiplaquetários.
A cirurgia de Ross parece ser, portanto, a cirurgia mais apropriada em crianças, adultos jovens e mulheres que desejem engravidar e, provavelmente, em pacientes que tenham uma expectativa de vida maior que 20 anos.